题目内容
如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中注入适量浓硫酸.
请回答:
(1)可观察到饱和澄清石灰水 ;
(2)U形管中a、b液面变化情况是 (选填序号).
A.a液面上升,b液面下降 B.a液面下降,b液面上升.

考点:
固体溶解度的影响因素;溶解时的吸热或放热现象.
专题:
溶液、浊液与溶解度.
分析:
(1)根据浓硫酸溶于水放出大量的热,结合氢氧化钙的溶解度随着温度的升高而减小,进行分析解答.
(2)根据浓硫酸溶于水放出大量的热,溶液温度升高,瓶内气体受热膨胀体积变大,据此进行分析解答.
解答:
解:(1)浓硫酸溶于水放出大量的热,溶液温度升高;结合氢氧化钙的溶解度随着温度的升高而减小,温度升高,氢氧化钙的溶解度减小,有氢氧化钙析出,则
观察到饱和澄清石灰水变浑浊.
(2)浓硫酸溶于水放出大量的热,溶液温度升高,瓶内气体受热膨胀体积变大,使U型管a液面下降,b液面上升.
故答案为:(1)变浑浊;(2)B.
点评:
本题难度不大,掌握浓硫酸溶于水放出热量、氢氧化钙的溶解度随着温度的升高而减小是正确解答本题的关键.

 阅读快车系列答案
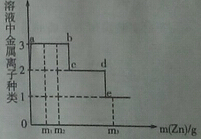
阅读快车系列答案如图表示的是KNO3和NaNO3的溶解度曲线,下列说法正确的是( )

|
| A. | T2℃时,KNO3溶液的浓度一定等于NaNO3溶液的浓度 |
|
| B. | T1℃时,在50g水里加入15g KNO3固体,充分溶解,可得到65g溶液 |
|
| C. | T1℃时,往180g NaNO3饱和溶液中加入620g水可配成质量分数为10%的NaNO3溶液 |
|
| D. | 若KNO3中混有少量NaNO3,可用蒸发溶剂的方法提纯 |
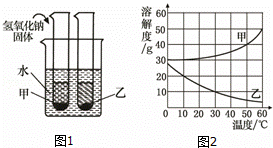
甲、乙两物质的溶解度曲线如图2所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯里,然后向烧杯中加入适量的氢氧化钠固体,搅拌至完全溶解(如图1),此时对相应变化的判断正确的是( )
|
| A. | 甲溶液可能变成不饱和溶液 |
|
| B. | 盛乙的试管中未溶解的固体质量减少 |
|
| C. | 甲、乙两物质的溶解度都增大 |
|
| D. | 乙溶液中溶质质量分数减小 |
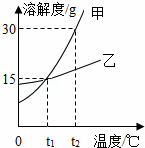
如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
|
| A. | 甲、乙两种物质的溶解度都不相等 |
|
| B. | 将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法 |
|
| C. | t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15% |
|
| D. | t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克 |
下表是NaCl和KNO3在不同温度时的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
|
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(1)从表中数据可以看出NaCl和KNO3的溶解度随温度升高而 (填“增大”或“减小”).
(2)若将KNO3的不饱和溶液变为相同温度下饱和溶液,其方法为 (填一种).若KNO3饱和溶液中含有少量NaCl时,提纯的方法是 (填一种).
(3)下列有关说法正确的是
A.40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大
B.KNO3饱和溶液中一定不能再溶解NaCl固体
C.从表中数据可以判断NaCl和KNO3的溶解度相等的温度在20﹣40℃之间.