题目内容
某化工厂的纯碱样品中含有少量的氯化钠。化学兴趣小组的同学为测定该纯碱样品中碳酸钠的含量,取该纯碱样品11g,全部溶解在80g水中,再加入170.7g 氯化钡溶液,恰好完全反应,过滤,得到19.7g沉淀(不考虑过滤过程中物质质量的损失)。请计算:
氯化钡溶液,恰好完全反应,过滤,得到19.7g沉淀(不考虑过滤过程中物质质量的损失)。请计算:
(1)纯碱样品中碳酸钠的质量。
(2)反应后所得溶液中溶质质量分数。
解法一:
解:设Na2CO3的质量为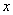 ,生成NaCl的质量为
,生成NaCl的质量为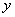
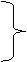 Na2CO3+ BaCl2 = BaCO3↓+ 2NaCl
Na2CO3+ BaCl2 = BaCO3↓+ 2NaCl
106 197 117 ……(1分)
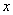 19.7g
19.7g 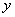
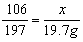
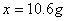 ……(1分)
……(1分) 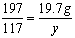
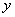 =11.7g ……(1分)
=11.7g ……(1分)
 反应后所得溶液中溶质的质量=11g-10.6g +11.7g = 12.1g
反应后所得溶液中溶质的质量=11g-10.6g +11.7g = 12.1g
|
反应后所得溶液中溶质质量分数= 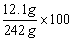 %=5%
%=5%
答:纯碱样品中碳酸钠的质量为10.6g,反应后所得溶液中溶质质量分数为5%。
解法二:
解:设Na2C O3的质量为
O3的质量为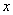 ,BaCl2的质量为
,BaCl2的质量为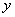 ,生成NaCl的质量为z
,生成NaCl的质量为z
 Na2CO3+ BaCl2 = BaCO3↓+ 2NaCl
Na2CO3+ BaCl2 = BaCO3↓+ 2NaCl
106 208 197 117 ……(1分)
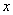
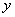 19.7g z
19.7g z
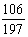 =
=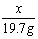
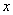 = 10.6g ……(1分)
= 10.6g ……(1分)
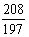 =
=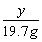
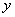 = 20.8g
= 20.8g
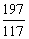 =
= 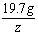 z = 11.7g
z = 11.7g

 反应后所得溶液中溶质的质量=11g-10.6g+11.7g=12.1g
反应后所得溶液中溶质的质量=11g-10.6g+11.7g=12.1g
反应后所得溶液的质量=80g+170.7g-20.8g+12.1g=242g
反应后所得溶液中溶质质量分数=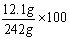 %=5% ……(1分)
%=5% ……(1分)
答:纯碱样品中碳酸钠的质量为10.6g,反应后所得溶液中溶质质量分数为5%。
(其它合理解法均可得分)

 某化工厂用侯氏制碱法制得的纯碱中含少量氯化钠.为了测定纯碱样品中碳酸钠的质量,化学兴趣小组的同学进行了以下实验:
某化工厂用侯氏制碱法制得的纯碱中含少量氯化钠.为了测定纯碱样品中碳酸钠的质量,化学兴趣小组的同学进行了以下实验: