题目内容
10.没有金属,生活是难以想象的,请你根据所学知识回答下列问题:(1)在一百余种元素中,金属元素的种类比非金属元素的种类多,现代社会以各种金属为支撑,其中用量最大、应用最广泛的金属是铁;
(2)我国早在春秋战国时期就开始炼铁、应用金属铁,现有200t含Fe2O380%的赤铁矿做原料,能生产含杂质4%的生铁116.7t;(结果保留至0.1).
(3)在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,充分反应后,铁粉有剩余,过滤,则滤液中一定没有的溶质是硫酸铜、硫酸,滤纸上一定含有的物质是铜、铁.
分析 (1)在一百余种元素中,金属元素的种类比非金属元素的种类多,现代社会以各种金属为支撑,其中用量最大、应用最广泛的金属是铁;
(2)根据物质的化学式及其提供的数据可以进行相关方面的计算;
(3)锌比铁活泼,铁比铜活泼.
解答 解:(1)在一百余种元素中,金属元素的种类比非金属元素的种类多,现代社会以各种金属为支撑,其中用量最大、应用最广泛的金属是铁.
故填:多;铁.
(2)反应过程中,氧化铁中的铁元素完全转化到生成的生铁中,能生产含杂质4%的生铁质量为:(200t×80%×$\frac{112}{160}$×100%)÷(1-4%)=116.7t,
故填:116.7t.
(3)在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,铁吧和硫酸锌反应,能和硫酸铜反应生成硫酸亚铁和铜,能和稀硫酸反应生成硫酸亚铁和氢气,充分反应后,铁粉有剩余,说明硫酸铜和硫酸都已经完全反应,则滤液中一定没有的溶质是硫酸铜和硫酸,过滤,滤纸上一定含有的物质是反应生成的铜和过量的铁.
故填:硫酸铜、硫酸;铜、铁.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
1.下列关于“化学之最”的说法中不正确的是( )
| A. | 相同条件下,密度最小的气体是氢气 | |
| B. | 最小的粒子是原子 | |
| C. | 天然存在最硬的物质是金刚石 | |
| D. | 人体中含量最多的物质是水 |
18.小明设计了下列四组物成,要求在一定条件下都能一步转化,其中错误的是( )
| A. | Na2CO3→NaCl→NaNO3→NaOH | B. | C→CO→Fe→Fe2O3 | ||
| C. | Cu→CuO→CuSO4→Cu(OH)2 | D. | CaCO3→CaO→Ca(OH)2→NaOH |
5.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证氯化钠溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
| D | 除去粗盐中的可溶性杂质 | 将粗盐研碎,溶解,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
2.现有含氯化钠的碳酸钠样品,为测定样品中氯化钠的含量.课外活动小组的同学称取20g该样品于烧杯中,并将80g稀盐酸评价分成四份,依次加入烧杯中,实验数据如表:
计算:
(1)产生CO2气体的总质量;
(2)样品中氯化钠的百分含量;
(3)使用的稀盐酸的溶质质量分数.
| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 反应后烧杯中剩余物质的质量/g | 37.8 | 55.6 | 74.5 | 94.5 |
(1)产生CO2气体的总质量;
(2)样品中氯化钠的百分含量;
(3)使用的稀盐酸的溶质质量分数.
20.下列实验操作中,“先”与“后”的顺序不正确的是( )
| A. | 制备气体时,先装药品,后检查装置的气密性 | |
| B. | 用排水法收集完氧气,先把导管移离水面,后停止加热 | |
| C. | 用量筒量取10mL液体时,先倒入接近10mL的液体,后用胶头滴管补至刻度线 | |
| D. | 以上说法都不对 |
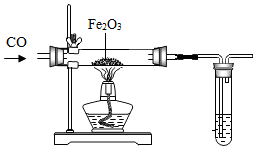 冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.
冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.