题目内容
13. 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:①将图中的集气瓶分为5等份,并作好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷需稍过量,目的是将集气瓶内的氧气全部消耗掉.
(2)步骤③中打开止水夹后观察到的现象是烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积的五分之一,由此可得氧气约为总体积的五分之一.
(3)写出红磷燃烧的符号表达式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(4)写出碳燃烧的符号表达式:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,结合符号表达式回答能否用木炭代上述探究实验:不可以(填“可以”或“不可以”),原因是木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化.
(5)该实验可推论出氮气难(填“易”或“难”)溶于水和不能(填“能”或“不能”)支持燃烧的结论.
分析 (1)红磷过量,能将瓶内的氧气全部消耗掉.
(2)根据瓶内压强的变化分析.
(3)红磷燃烧生成了五氧化二磷,根据反应写出反应的方程式;
(4)根据化学方程式的书写方法、步骤进行书写即可;根据木炭燃烧的产物结合压强知识进行解答;
(5)氮气难溶于水,也不能与水发生反应、不燃烧、也不支持燃烧.
解答 解:(1)红磷需稍过量,目的是:将集气瓶内的氧气全部消耗掉;故填:将集气瓶内的氧气全部消耗掉;
(2)由于红磷燃烧生成了五氧化二磷固体,消耗了瓶内的氧气,瓶内的压强减小.所以,冷却后,松开止水夹,你观察到的现象为:烧杯里的水倒吸到集气瓶内(或烧杯的水面下降),集气瓶中的水约占集气瓶容积的五分之一,由此可以得出:空气中氧气的体积分数的五分之一;故填:烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积的五分之一;五分之一;
(3)红磷燃烧生成了五氧化二磷,反应写出反应的方程式是:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(4)碳在氧气中燃烧生成了二氧化碳,故可以写出该反应的化学方程式:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化,所以实验失败;故填:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;不可以;木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化;
(5)水进入瓶内占五分之一.不再继续进入说明氮气不能与红磷反应,也不能溶于水或与水反应;红磷熄灭说明氮气不燃烧也不支持燃烧,故填:难;不能.
点评 熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案| A. |  纸张燃烧 | B. |  雕刻石像 | C. |  葡萄酿酒 | D. |  铁钉生锈 |
| A. | 冰雪融化 铁丝燃烧 | B. | 铁器生锈 干冰升华 | ||
| C. | 木柴燃烧 矿石炼铁 | D. | 酒精挥发 光合作用 |

| A. | X一定是稀盐酸 | B. | 酚酞溶液遇X溶液变红色 | ||
| C. | Y溶液是中性溶液 | D. | Z溶液能使石蕊溶液变红 |
| A. | 稀硫酸除铁锈:FeO+H2SO4═FeSO4+HO2 | |
| B. | 一氧化碳还原氧化铁Fe2O3+3CO═2Fe+3CO2↑ | |
| C. | 从废液中提取银:Zn+2AgNO3═Zn(NO3)2+2Ag | |
| D. | 加热氯化钾制取氧气:KClO3$\frac{\underline{\;\;△\;\;}}{\;}$KCl+O2↑ |
| A. | 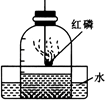 | B. | 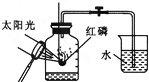 | C. |  | D. | 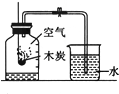 |