题目内容
17.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作或方法中正确的是( )| A. | 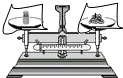 称固体质量 | B. | 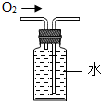 收集氧气 | C. | 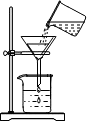 过滤 | D. | 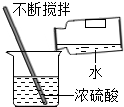 稀释浓硫酸 |
分析 A、根据托盘天平的使用分析.
B、根据氧气的收集方法进行分析判断.
C、过滤液体时,要注意“一贴、二低、三靠”的原则.
D、根据浓硫酸的稀释方法进行分析判断.
解答 解:A、托盘天平应该遵循“左物右码”,图中所示操作正确.
B、收集氧气用排水法收集,图中所示操作正确.
C、过滤液体时,要注意“一贴、二低、三靠”的原则,用玻璃棒引流,图中所示操作错误.
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
故选:B
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
7.一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟.事故路面上洒落了五六百米燃着的石头,这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼.大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应的可燃性气体可能是:氧气、氢气或乙炔(C2H2),同学们做出以上猜想的理论依据是化学反应前后元素的种类不变,大家讨论后一致认为该气体不可能是氧气,原因是氧气不具有可燃性;
电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙中的一种.同学们经过讨论认为白色固体不可能是氧化钙,因为氧化钙会与水反应.
【实验探究】
【反思交流】请根据以上实验结论写出电石与水反应的化学方程式CaC2+2H2O=C2H2↑+Ca(OH)2,载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是放热(填“吸热”或“放热”)反应.
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应的可燃性气体可能是:氧气、氢气或乙炔(C2H2),同学们做出以上猜想的理论依据是化学反应前后元素的种类不变,大家讨论后一致认为该气体不可能是氧气,原因是氧气不具有可燃性;
电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙中的一种.同学们经过讨论认为白色固体不可能是氧化钙,因为氧化钙会与水反应.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃 | 气体燃烧,产生黄色火焰并伴有浓烈黑烟 | 电石与水反应产生的气体是乙炔(C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸 | 固体溶解,没有气泡产生 | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后的固体于试管中加水,向上层清液中滴加酚酞 | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
8.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 酒精作燃料 C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O 氧化反应 | |
| B. | 高炉炼铁 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 | |
| C. | 用氢氧化钠溶液吸收二氧化碳 CO2+2NaOH═Na2CO3+H2O 复分解反应 | |
| D. | 实验室制取氧气 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ 分解反应 |
12.Fe2O3、CuO的固体混合粉末a g,高温下用足量氢气还原,得到金属混合物4.80g,将生成的水用足量的浓硫酸吸收后,浓硫酸增重1.8克,则a的值为( )
| A. | 6.40 | B. | 6.60 | C. | 8.00 | D. | 8.40 |
6.空气质量事关人类生存质量,PM2.5也是空气中污染物之一,要加强监测,采取措施,确保指数达标,关于PM2.5产生的原因分析不正确的是( )
| A. | 火力发电 | B. | 焚烧垃圾 | C. | 建筑粉尘 | D. | 白色污染 |
7.某工厂利用熟石灰除去废液中残余的盐酸,使废液呈中性而达到排放标准.某校化学兴趣小组成员取处理后的废液样品进行检测.
【提出问题】样品中的溶质是什么?
【作出猜想】猜想一:只有CaCI2;
猜想二:可能是CaCl2和Ca(OH)2
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【进行实验】甲、乙两位同学用不同类别的试剂进行实验,得到同样结论.
【反思与评价】
(1)用熟石灰除去废液中残余盐酸的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
(2)为避免这种不符合排放标准的结果出现,你认为处理废液中残余盐酸时,可以使用过量的石灰石.
【提出问题】样品中的溶质是什么?
【作出猜想】猜想一:只有CaCI2;
猜想二:可能是CaCl2和Ca(OH)2
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【进行实验】甲、乙两位同学用不同类别的试剂进行实验,得到同样结论.
| 实验步骤 | 实验现象 | 实验结论 | |
| 甲 | 取少量样品于试管中,滴入几滴无色酚酞溶液 | 溶液由无色变红色 | 猜想二正确 |
| 乙 | 取少量样品于试管中,加入硫酸铜溶液(或通入二氧化碳) | 有蓝色沉淀产生(或产生白色沉淀) |
(1)用熟石灰除去废液中残余盐酸的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
(2)为避免这种不符合排放标准的结果出现,你认为处理废液中残余盐酸时,可以使用过量的石灰石.
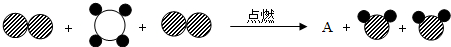
 ”表示碳原子,“
”表示碳原子,“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,该生成物A为
”表示氧原子,该生成物A为