题目内容
12.Fe2O3、CuO的固体混合粉末a g,高温下用足量氢气还原,得到金属混合物4.80g,将生成的水用足量的浓硫酸吸收后,浓硫酸增重1.8克,则a的值为( )| A. | 6.40 | B. | 6.60 | C. | 8.00 | D. | 8.40 |
分析 反应为:Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O,CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,根据反应方程式判断H2O中的O原子来源于金属氧化物,H2O中的氧元素的质量等于金属氧化物中氧元素的质量,计算出氧化物中氧元素的质量,金属氧化物的质量等于金属的质量加氧化物中氧元素的质量.
解答 解:0.9克水中氧元素的质量=1.8g×$\frac{16}{18}$×100%=1.6g,
所以金属氧化物的质量为4.8g+1.6g=6.4g,即a=6.4.
故选:A.
点评 本题考查混合物的质量计算,题目难度不大,注意从元素质量守恒的角度分析,关键是确定H2O的物质的量等于金属氧化物中氧原子的物质的量.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
2.下列各组物质,能在pH=1.5的溶液中大量共存,且形成无色溶液的是( )
| A. | NaCl AlCl3 Na2SO4 | B. | Na2CO3 NaCl Na2SO4 | ||
| C. | CuSO4 NaCl NaNO3 | D. | Na2SO4 NaOH KCl |
3.如图表示治理汽车尾气所涉及反应的微观过程,下列说法正确的是( )
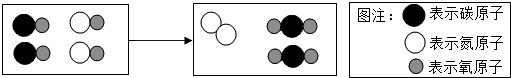

| A. | 图中单质的化学式为O2 | |
| B. | 该反应使有害气体转化为无害气体 | |
| C. | 生成物中的CO2属大气污染物 | |
| D. | 化学反应前后分子种类和个数都不改变 |
7.党的十八大报告中把“生态文明建设”首次提升到更高的战略层面,要求加大自然生态系统和环境保护力度.下列做法不符合这一要求的是( )
| A. | 加快污染治理型环保产业的发展 | |
| B. | 为缓解电力紧张各地可自行建设火力发电厂 | |
| C. | 大力宣传垃圾分类回收 | |
| D. | 研发易降解的生物农药和塑料 |
17.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作或方法中正确的是( )
| A. | 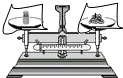 称固体质量 | B. | 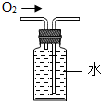 收集氧气 | C. | 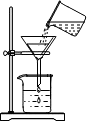 过滤 | D. | 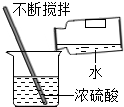 稀释浓硫酸 |
1.对比实验是一种常用的实验方法.下列实验不属于对比实验的是( )
| A. | 探究铁钉锈蚀的条件 | B. | 探究二氧化碳与水的反应 | ||
| C. | 用盐酸探究铁、铜的活动性强弱 | D. | 探究空气中氧气的含量 |

 在某种硬水中含有的钙、镁化合物为Ca(HCO3)2和Mg(HCO3)2,在加热煮沸时,两种可溶性物质会完全分解产生水垢,水垢的成分是CaCO3和Mg(OH)2.为了测定某种硬水中含钙镁化合物的质量,将一定质量的硬水加热蒸干后得到15.8g水垢,将此水垢加入100g稀盐酸恰好完全反应,测得烧杯中所盛物质的质量随时间变化的关系如图所示:
在某种硬水中含有的钙、镁化合物为Ca(HCO3)2和Mg(HCO3)2,在加热煮沸时,两种可溶性物质会完全分解产生水垢,水垢的成分是CaCO3和Mg(OH)2.为了测定某种硬水中含钙镁化合物的质量,将一定质量的硬水加热蒸干后得到15.8g水垢,将此水垢加入100g稀盐酸恰好完全反应,测得烧杯中所盛物质的质量随时间变化的关系如图所示: