题目内容
18.用2000吨含Fe2O380%的赤铁矿石,理论上可以炼出含铁96%的生铁多少吨?分析 赤铁矿石中氧化铁与一氧化碳在高温下反应生成铁和二氧化碳,根据该反应的化学方程式可确定反应中氧化铁与生成铁的质量关系,利用这一质量关系可由矿石中氧化铁的质量计算反应生成铁的质量,然后利用生铁中铁的含量求出炼出铁的质量.
解答 解:2000t矿石中含氧化铁的质量为:2000t×80%=1600t,
设1600t氧化铁理论上可炼出铁的质量为x
Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
1600t x
$\frac{160}{112}=\frac{1600t}{x}$ 解得:x=1120t
则含铁96%的生铁的质量为:1120t÷96%=1166.7t
答:理论上可以炼出含铁96%的生铁1166.7t.
点评 根据化学方程式进行计算时,所使用物质的质量均是纯净物的质量,不能直接使用不纯净的物质的质量进行计算.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
8.下列判断正确的是( )
| A. | 合金至少由两种金属熔合而成 | |
| B. | 不同种元素最本质的区别是质子数不同 | |
| C. | 饱和溶液变成不饱和溶液,其溶质质量分数一定变小 | |
| D. | 两种化合物相互作用生成另外两种化合物的反应一定是复分解反应 |
6. 小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )
小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )
 小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )
小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…下列关系中,有错误的一组是( )| 甲 | 乙、丙、丁… | |
| A | 盐 | 食盐、纯碱、高锰酸钾… |
| B | 合金 | 不锈钢、焊锡、生铁… |
| C | 溶液 | 碘酒、糖水、生理盐水… |
| D | 干燥剂 | 石灰石、浓硫酸、烧碱… |
| A. | A | B. | B | C. | C | D. | D |
13. 2010年诺贝尔物理学奖授予了英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫.共同工作多年的二人因成功获得超薄材料石墨烯而获奖.石墨烯是从石墨材料中剥离出来的由碳原子组成的物质(如图),是目前已知的世界上强度最高的材料.根据你所学的知识,可推断石墨烯应属于( )
2010年诺贝尔物理学奖授予了英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫.共同工作多年的二人因成功获得超薄材料石墨烯而获奖.石墨烯是从石墨材料中剥离出来的由碳原子组成的物质(如图),是目前已知的世界上强度最高的材料.根据你所学的知识,可推断石墨烯应属于( )
 2010年诺贝尔物理学奖授予了英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫.共同工作多年的二人因成功获得超薄材料石墨烯而获奖.石墨烯是从石墨材料中剥离出来的由碳原子组成的物质(如图),是目前已知的世界上强度最高的材料.根据你所学的知识,可推断石墨烯应属于( )
2010年诺贝尔物理学奖授予了英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫.共同工作多年的二人因成功获得超薄材料石墨烯而获奖.石墨烯是从石墨材料中剥离出来的由碳原子组成的物质(如图),是目前已知的世界上强度最高的材料.根据你所学的知识,可推断石墨烯应属于( )| A. | 混合物 | B. | 单质 | C. | 化合物 | D. | 合金 |
3.某同学欲选用下列几组试剂探究 Al、Fe、Cu 三种金属的活动性顺序,其中不能达到目的是( )
| A. | Fe、Cu、Al2(SO4)3 溶液 | B. | Al、Cu、FeSO4 溶液 | ||
| C. | Fe、Al2(SO4)3溶液、CuSO4 溶液 | D. | Al、Fe、Cu、稀 H2SO4 |
16.化学兴趣小组的同学对实验氧气的制取进行了如图探究.
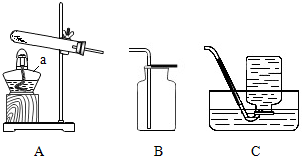
(1)仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.用装置A、C制取氧气,收集完氧气时,应进行的操作是先将导管移出水面,再熄灭酒精灯.
(3)在老师指导下,同学们对一个化学反应可能有多种催化剂的问题进行了探究.
【提出猜想】除二气化锰(MnO2)外,氧化铜(CuO)、氧化铁(Fe2O3)也可以作氯酸钾(KClO3)
分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
【分析与结论】对比实验①与④,可知氧化铁可加快氯酸钾分解的速率; 实验所用的三种
物质,催化效果最好的是二氧化锰.
【反思与拓展】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质 不变; 同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.

(1)仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.用装置A、C制取氧气,收集完氧气时,应进行的操作是先将导管移出水面,再熄灭酒精灯.
(3)在老师指导下,同学们对一个化学反应可能有多种催化剂的问题进行了探究.
【提出猜想】除二气化锰(MnO2)外,氧化铜(CuO)、氧化铁(Fe2O3)也可以作氯酸钾(KClO3)
分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度/℃ |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比1:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
物质,催化效果最好的是二氧化锰.
【反思与拓展】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质 不变; 同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.
| 实验步骤 | 实验现象 | 实验结论 |
| 小颗粒的分解温度为380℃, 大颗粒的分解温度为390℃ |