题目内容
13.氢气和氧气的混合气体10克,点燃充分反应后冷却,瓶中剩余1克气体,则原混合物中氢气和氧气的质量分别为( )| A. | 可能是2克氢气和8克氧气 | B. | 一定是1克氢气和9克氧气 | ||
| C. | 可能是5克氢气和5克氧气 | D. | 一定是4克氢气和6克氧气 |
分析 根据题意在分析已知量和未知量之间的质量关系时,要注意找出隐蔽的条件.对于该题已知生成物的质量,根据化学方程式可求出反应物的质量.
解答 解:设参加反应的氢气为x,氧气的质量为y;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 32 36
x y 9g
$\frac{4}{x}$=$\frac{32}{y}$=$\frac{36}{9g}$
解得:x=1g y=8g
因为氢气和氧气的混合气体共10g,充分反应后生成9g水,根据质量守恒定律和计算可知可知参加反应的氢气为1g,氧气为9g;所以肯定其中有一种物质过量.①当氢气为1g时,则氧气为10-1=9g;②当氧气为8g时,则氢气的质量为10-8=2g
故选:A.
点评 根据化学方程式的计算,必须对有关的化学知识有清晰的理解,熟练掌握有关反应的化学方程式.

练习册系列答案
相关题目
3.在科学学习过程中,常常要用到分类的方法.下列各组物质的分类正确的是( )
| A. | 混合物:空气 粗盐 牛奶 | B. | 盐:氯化钙 硫酸 硝酸钾 | ||
| C. | 氧化物:MgO P2O5 KClO3 | D. | 单质:铝 金刚石 氯化氢 |
2. 如图是气体X的干燥、收集、尾气吸收装置,该气体可能的物理性质是( )
如图是气体X的干燥、收集、尾气吸收装置,该气体可能的物理性质是( )
 如图是气体X的干燥、收集、尾气吸收装置,该气体可能的物理性质是( )
如图是气体X的干燥、收集、尾气吸收装置,该气体可能的物理性质是( )| A. | 密度比空气大,极易溶于水 | B. | 密度比空气小,极易溶于水 | ||
| C. | 密度比空气大,难溶于水 | D. | 密度比空气小,难溶于水 |

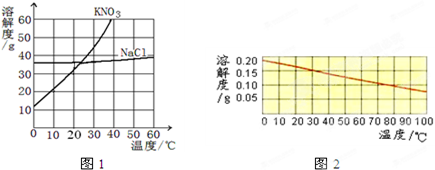
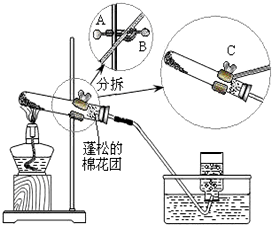 某同学做“高锰酸钾制取氧气”的实验过程如下:
某同学做“高锰酸钾制取氧气”的实验过程如下: