题目内容
18.下列说法不正确的是( )| A. | 锅炉用水硬度高了十分危险 | |
| B. | 煮沸水可以降低水的硬度 | |
| C. | 水垢是水中可溶性钙和镁的化合物加热后生成的沉淀 | |
| D. | 静置沉淀可以使硬水软化 |
分析 A、根据硬水对锅炉的影响进行分析;
B、根据硬水软化的方法进行分析;
C、根据水垢形成的原理进行分析;
D、根据静置沉淀的原理进行分析.
解答 解:A、硬水中含有较多的可溶性钙镁化合物,可溶性钙镁化合物受热易转化生成不溶性钙镁化合物,形成水垢,水垢在锅炉内壁附着,不仅浪费燃料,而且也由于受热不均匀,可能引起爆炸,故说法正确.
B、加热煮沸时,水中的钙离子能够以碳酸钙的形式从水中析出,镁离子能够以氢氧化镁的形式从水中析出,所以加热煮沸可以降低水的硬度,故说法正确.
C、水垢是水中可溶性钙和镁的化合物加热后生成的沉淀,故说法正确.
D、硬水是因为水中含有较多的钙离子、镁离子,通过静置沉淀不能除去钙离子和镁离子,即不能软化硬水,故说法不正确.
故选:D.
点评 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,是中考热点之一.

练习册系列答案
相关题目
9.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与NaOH 溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与NaOH 溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
6.欲除去一氧化碳中少量的二氧化碳,最好的方法是( )
| A. | 使混合气体在空气中点燃 | |
| B. | 使混合气体通过灼热的氧化铜 | |
| C. | 使混合气体通过澄清石灰水 | |
| D. | 将集气瓶口朝下,移开玻璃片使二氧化碳气体自动逸出 |
10.下列关于物质在氧气中燃烧的实验现象描述正确的是( )
| A. | 石蜡在氧气中燃烧时,有水和二氧化碳生成 | |
| B. | 镁在氧气中燃烧时,发出耀眼的强光,生成黑色固体 | |
| C. | 木炭在氧气中燃烧时,火焰呈黄色,产生大量白烟 | |
| D. | 铁丝在氧气中燃烧时,火星四射,有黑色固体生成 |
8.将深色的衣服和浅色的衣服浸泡在一起,会使浅色衣服染上深颜色,这其中的主要原因是由于深色染料中的( )
| A. | 分子是在不断地运动 | B. | 分子本身发生了改变 | ||
| C. | 分子间的间隔增大 | D. | 分子在化学变化中发生变化 |
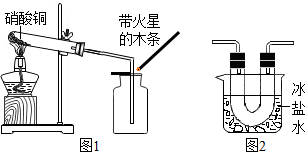 硝酸铜为蓝色固体,水溶液为蓝色,某小组用图1装置加热硝酸铜,观察到固体由蓝色逐渐变黑,产生红棕色气体,带火星的木条复燃.
硝酸铜为蓝色固体,水溶液为蓝色,某小组用图1装置加热硝酸铜,观察到固体由蓝色逐渐变黑,产生红棕色气体,带火星的木条复燃.