题目内容
将
4.6g某化合物放入氧气中完全燃烧,生成8.8g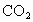 和5.4g
和5.4g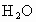 .问:这种化合物里含有哪几种元素?4.6g该化合物中各元素的质量分别是多少?
.问:这种化合物里含有哪几种元素?4.6g该化合物中各元素的质量分别是多少?
答案:略
解析:
解析:
|
4.6g 该化合物中含C、H元素的质量分别为:碳: 8.8g×12÷44=2.4g氢: 5.4g×2÷18=0.6g显然 4.6g>(2.4+0.6)g,根据质量守恒定律可知,该化合物还含有氧元素,其质量为:4.6g-2.4g-0.6g=1.6g因此,该化合物中含有 C、H、O三种元素,4.6g该化合物中各元素的质量分别为2.4g、0.6g、1.6g.本题属于根据已知的生成物的质量求反应物元素种类和质量的问题.由质量守恒定律可知,该化合物中肯定含有 C、H两种元素,且与生成的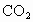 和 和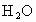 中所含的C、H两种元素的质量相等.这样,便可,迅速算出4.6g该化合物中C、H元素的质量,然后再与该化合物的总质量相比,即可知是否含有O元素,并计算出其质量. 中所含的C、H两种元素的质量相等.这样,便可,迅速算出4.6g该化合物中C、H元素的质量,然后再与该化合物的总质量相比,即可知是否含有O元素,并计算出其质量. |

练习册系列答案
相关题目