题目内容
11.以下说法正确的是AEF.A.人体内缺钙会导致疏松症; B.用甲醛溶液浸泡水产品,可以起到防腐作用;
C.常用钢丝球擦洗铝壶可以使其光亮洁净且耐用;D.将工业明胶代替食用明胶,添加到老酸奶中;
E.蚕丝所含成分为蛋白质;F.可以用燃烧闻气味的方法区别羊毛和丝棉.
分析 A、根据人体缺钙会导致骨质疏松分析;
B、根据甲醛有毒进行解答;
C、根据用钢丝球擦洗会破坏致密的氧化物保护膜进行分析判断;
D、根据工业明胶含有一些重金属,使人中毒进行解答;
E、根据蚕丝的成份分析解答;
F、根据区别羊毛和丝棉的方法进行解答.
解答 解:A、人体缺钙会导致骨质疏松,故正确;
B、甲醛有毒,不能用甲醛溶液浸泡水产品,故错误;
C、铝锅表面有一层致密的氧化物薄膜,对铝锅起到保护作用,如果用钢丝球擦洗,可能把氧化物薄膜擦去,破坏了其表面的氧化膜,故错误;
D、工业明胶含有一些重金属,能使人中毒,所以不能用废弃的皮鞋等废旧物生产工业明胶代替食用明胶添加到老酸奶、果冻中,故错误;
E、蚕丝的成份主要是蛋白质,正确.
F、纯羊毛的成分为蛋白质,灼烧有烧焦羽毛的气味;纯棉织物中不含有蛋白质,灼烧时没有烧焦羽毛的气味.正确.
故选:AEF.
点评 解答本题要掌握各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
6.如图的图象与对应的实验过程不相符的是( )
| A. |  将锌片插入盛有一定质量的稀硫酸的烧杯中 | |
| B. |  向一定量的表面含有氧化铝的铝片滴加稀硫酸 | |
| C. |  正二价金属与一定量的稀硫酸反应,由图象可知,金属M比金属N相对原子质量小 | |
| D. |  向一定量的Ba(OH)2溶液中加入Na2SO4粉末 |
16.下列化学实验操作中正确的是( )
| A. | 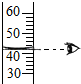 量取液体 | B. | 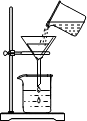 过滤 | C. | 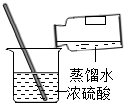 稀释浓硫酸 | D. | 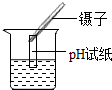 检测溶液pH |
3.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 金刚石和石墨都是碳的单质,金刚石很硬,故石墨也很硬 | |
| B. | 合金比组成它的纯金属硬,故黄铜比纯铜硬 | |
| C. | 稀硫酸能和氯化钡反应生成白色沉淀,故稀盐酸也可以 | |
| D. | 氢氧化镁和氢氧化钠都是碱,氢氧化镁可以治疗胃酸过多,故氢氧化钠也可以 |
20.如图是甲乙两位同学在学习碳酸钠的化学性质时所做的探究实验.
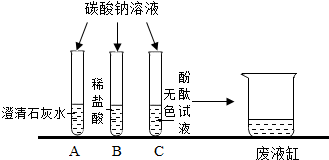
(1)A 中发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)B中发生化学反应的实质是氢离子与碳酸根离子反应生成水分子和二氧化碳分子.
(3)C中观察到的现象是酚酞试液变红色.
(4)将A、B、C三支试管内反应后的物质倒入废液缸中,发现废液澄清有气泡冒出,且酚酞溶液呈无色.
【提出问题】最终溶液中含有什么溶质?
【猜想与假设】
甲同学的猜想:废液中有氯化钙和氯化钠;
乙同学的猜想:废液中有氯化钙、氯化钠和氯化氢;
【活动与探究】为了验证甲、乙两位同学的猜想请你设计实验.
【交流反思】
最终废液的正确处理方法是加入适量熟石灰中和后排放.

(1)A 中发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)B中发生化学反应的实质是氢离子与碳酸根离子反应生成水分子和二氧化碳分子.
(3)C中观察到的现象是酚酞试液变红色.
(4)将A、B、C三支试管内反应后的物质倒入废液缸中,发现废液澄清有气泡冒出,且酚酞溶液呈无色.
【提出问题】最终溶液中含有什么溶质?
【猜想与假设】
甲同学的猜想:废液中有氯化钙和氯化钠;
乙同学的猜想:废液中有氯化钙、氯化钠和氯化氢;
【活动与探究】为了验证甲、乙两位同学的猜想请你设计实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量废液于试管中,向其中加入. | 有气泡冒出 | 乙同学猜想正确 |
最终废液的正确处理方法是加入适量熟石灰中和后排放.
1.图象和表格是数据表达的重要手段,根据下列图表回答问题.

表一 甲、乙分别在水、酒精中的溶解度
(1)分析表一数据可知,物质的溶解度受BCD(填序号)的影响.
A.溶剂质量 B.溶剂性质 C.溶质性质 D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全 B.数据更精准 C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.

表一 甲、乙分别在水、酒精中的溶解度
| 甲 | 乙 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |
A.溶剂质量 B.溶剂性质 C.溶质性质 D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全 B.数据更精准 C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.