题目内容
归纳推理是学习化学的重要方法之一.下列有关事实和推理得到的结论合理的是( )
| 事实 | 结论 | |
| A | 二氧化锰对氯酸钾分解和过氧化氢分解均有催化作用 | 不同的反应有时可以使用同一种物质作催化剂 |
| B | 白磷和红磷均是由磷元素组成的单质 | 白磷和红磷属于同一种物质 |
| C | C与O2反应能放出大量的热 | C与O2不需要任何条件就可以发生反应 |
| D | Al在常温下就能与O2发生发应,Fe在常温下几乎不与O2反应 | Al的抗腐蚀性能比Fe弱 |
A.A B.B C.C D.D
【分析】A、据催化剂的特点解答此题;
B、红磷和白磷是同种元素组成的不同单质,属同素异形体;
C、据碳与氧气的反应条件是点燃解答此题;
D、据铝与铁的化学性质,在潮湿的空气中,铁与氧气发生缓慢氧化而生成铁锈,铁锈呈红色,结构疏松,易吸水,加快铁器的腐蚀,铝在空气容易形成致密的氧化物,故其抗腐蚀性能很好.
【解答】解:A、据催化剂的特点“一变,两不变”,即能改变化学反应的速率,而本身的质量和化学性质不变,二氧化锰对氯酸钾分解和过氧化氢分解均有催化作用,故得出结论:不同的反应有时可以使用同一种物质作催化剂,故A合理;
B、红磷和白磷是同种元素组成的不同单质,属同素异形体,不是同一种物质,故B不合理;
C、据碳常温时,具有稳定性,点燃时,具有可燃性,知碳与氧反应需点燃,而不是C与O2不需要任何条件就可以发生反应,故C不合理;
D、据铝与铁的化学性质,在潮湿的空气中,铁与氧气发生缓慢氧化而生成铁锈,铁锈呈红色,结构疏松,易吸水,加快铁器的腐蚀,铝在空气容易形成致密的氧化物,故其抗腐蚀性能很好,故D不合理.
故选A.

 阅读快车系列答案
阅读快车系列答案硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)和副产物石膏(CaSO4•2H2O)的生产流程示意图:
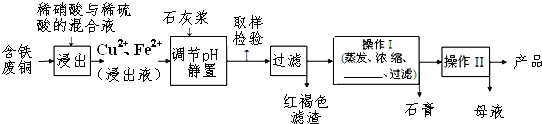
胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是 ;
(2)含铁的废铜和稀硫酸反应的化学方程式 F ;
(3)操作I最后温度应该控制在 ℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、 、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 .







