题目内容
根据二氧化碳的化学式计算:
①CO2的相对分子质量;
②二氧化碳里碳元素与氧元素的质量比,
③二氧化碳里碳元素的质量分数?
④22g二氧化碳里含有碳元素多少克?
①CO2的相对分子质量;
②二氧化碳里碳元素与氧元素的质量比,
③二氧化碳里碳元素的质量分数?
④22g二氧化碳里含有碳元素多少克?
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:①根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
②根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
③根据化合物中元素的质量分数公式进行分析解答.
④根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析解答.
②根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
③根据化合物中元素的质量分数公式进行分析解答.
④根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析解答.
解答:解:①二氧化碳的相对分子质量为12+16×2=44;
②二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8;
③二氧化碳含有碳元素的质量分数是
×100%≈27.3%;
④11克里二氧化碳含有碳元素的质量为22g×
×100%=6g;
故答案为:①CO2的相对分子质量是44;
②二氧化碳里碳元素与氧元素的质量比是3:8;
③二氧化碳里碳元素的质量分数是27.3%;
④22g二氧化碳里含有碳元素6g.
②二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8;
③二氧化碳含有碳元素的质量分数是
| 12 |
| 12+16×3 |
④11克里二氧化碳含有碳元素的质量为22g×
| 12 |
| 12+16×3 |
故答案为:①CO2的相对分子质量是44;
②二氧化碳里碳元素与氧元素的质量比是3:8;
③二氧化碳里碳元素的质量分数是27.3%;
④22g二氧化碳里含有碳元素6g.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
用MgO、Mg、Mg(OH)2、稀硫酸、CuSO4五种物质两两反应,得到MgSO4的方法有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列关于试剂的取用操作中,不正确的是( )
| A、用胶头滴管吸收少量试剂 |
| B、用镊子夹取块状固体 |
| C、用酒精灯外焰给物质加热 |
| D、实验室用剩的药品不能乱放,一定要放回原试剂瓶中 |
一种元素与另一种元素最本质的区别是( )
| A、核电荷不同 |
| B、原子量不同 |
| C、核外电子数不同 |
| D、中子数不同 |
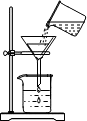 (1)区别硬水和软水的一种简单的方法是
(1)区别硬水和软水的一种简单的方法是 我市鄂伦春旗大杨树镇产天然矿泉水商标的部分内容如图所示,请仔细阅读并完成下列各题.
我市鄂伦春旗大杨树镇产天然矿泉水商标的部分内容如图所示,请仔细阅读并完成下列各题.