题目内容
5.目前,我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础.(一)铁的广泛应用
(1)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理Fe+CuSO4=FeSO4+Cu.
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料.以上叙述中不涉及到B(选填序号).
A.合金 B.无机非金属材料 C.合成材料 D.复合材料
(二)铁锈成分的探究
(3)如图为某兴趣小组探究铁生锈的三个实验,
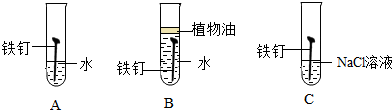
最先观察到铁锈的是C(选填序号).
(4)铁锈组分的确定
某铁锈成分为Fe2O3•xH2O和FeCO3.为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下用如图装置进行实验.

【查阅资料】①Fe2O3•xH2O多余空温度为110℃,FeCO3在282℃分解为FeO和CO2.②温度高于500℃时铁的氧化物才能被CO还原.
①装置A中的反应为:H2C2O4(草酸)CO↑+CO2↑+H2O.通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放c(选填序号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
②现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重3.6g,装置F增重2.2g.
则样品中FeCO3的质量m(FeCO3)=5.8g,x=2.
分析 (一)(1)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(2)根据材料的分类解答;
(二)(3)根据铁生锈的条件进行解答;
(4)根据铁与水和氧气作用下生成氢氧化亚铁进行分析;
①根据草酸分解生成水、二氧化碳、一氧化碳,在一氧化碳参与反应之前,需要先将二氧化碳和水除去进行分析;
③根据浓硫酸有吸水性,碱石灰会与二氧化碳反应进行分析;
解答 解:(一)(1)硫酸铜溶液遇到金属铁时,铁与硫酸铜发生置换反应能生成金属铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;
(2)不锈钢丝属于金属材料,聚乙烯纤维属于合成材料,耐酸防护服材料属于复合材料,故选:B;
(二)(3)铁生锈时,需要水分和氧气同时存在,当有盐类物质存在时,生锈速度加快,故选:C;
(4)①依据质量守恒定律可知,生成物中有氢元素,所以反应物中也必须有氢元素,草酸H2C2O4分解生成水、二氧化碳、一氧化碳,在一氧化碳参与反应之前,需要先将二氧化碳和水除去,浓硫酸有吸水性,氢氧化钠会与二氧化碳反应,要先除二氧化碳,在除水蒸气,所以洗气瓶B中应盛放氢氧化钠溶液,故选:c;
②浓硫酸有吸水性,碱石灰会与二氧化碳反应,加热到了300℃,所以一氧化碳不会还原氧化铁,浓硫酸增加的质量是水的质量,来自铁锈,碱石灰增加的质量来自碳酸亚铁分解生成的二氧化碳,所以依据元素守恒进行计算
设碳酸亚铁的质量为y,$\frac{12}{116}$×y=$\frac{12}{44}$×2.2g,y=5.8g,
所以Fe2O3•xH2O为:25.4g-5.8g=19.6g,氧化铁的质量为:$\frac{160}{196}$×19.6g=16g,$\frac{2x}{160+18x}$×19.6g=$\frac{2}{18}$×3.6g,解得x=2;
故答案为:
(一)(1)Fe+CuSO4=FeSO4+Cu;(或其它可溶性铜盐与铁反应)(2)B;
(二)(3)C;(4)①c; ②5.8; 2
点评 本题考查一氧化碳还原铁的氧化物的步骤、现象、化学反应式的书写,以及用不同的方法验证铁的存在,需要同学们具有比较全面的化学知识.

| A. | 水是由氢、氧两种元素组成的化合物 | |
| B. | 自来水是一种纯净物 | |
| C. | 用肥皂水可以区别硬水和软水 | |
| D. | 海水是混合物 |
| A. | NaOH NaC1 CuSO4 HC1 | B. | KNO3 Na2SO4 NaOH KC1 | ||
| C. | KC1 Ba(NO3)2 HC1 CaC12 | D. | Na2CO3 Ba(OH)2 KNO3 Na2SO4 |


 已知A,B,C,D,E是初中化学中常见的五种物质,气体D能使澄清石灰水变浑浊,它们之间有如图所示的转化关系
已知A,B,C,D,E是初中化学中常见的五种物质,气体D能使澄清石灰水变浑浊,它们之间有如图所示的转化关系