题目内容
20.在复习氧气、二氧化碳和氢气的制取和性质时,某兴趣小组同学利用以下装置进行了气体制取和性质的研究.
(1)写出图中标号①的仪器名称:长颈漏斗;
(2)为验证气体的性质,小露将制取的气体通入H装置中,能观察到H中有气泡逸出且溶液变浑浊,则该气体是从a(选填“a”或“b”)通入装置H的,产生该气体的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,小露制取该气体选择的发生装置是一套能随时控制反应发生和停止的装置,则该装置是(填序号)B;
(3)小明用一套发生装置和装置E制取氧气时,发现水槽中的水变红了,则他制取该气体的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择A(填序号).甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图I所示,据此可推断甲烷一定具备的物理性质是:难溶于水、密度比空气小.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;检验二氧化碳气体要长进短出,B装置的优点是能随时控制反应发生和停止;实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图I所示,据此可推断甲烷一定具备的物理性质是:难溶于水、密度比空气小.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;检验二氧化碳气体要长进短出,B装置的优点是能随时控制反应发生和停止;故答案为:a、CaCO3+2HCl═CaCl2+H2O+CO2↑、B;
(3)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,因此需要加热;甲烷气体一般采用装置E进行收集,收集满后集气瓶的放置方式如图I所示,据此可推断甲烷一定具备的物理性质是:难溶于水、密度比空气小;故答案为:A、难溶于水、密度比空气小;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 吃进的食物一段时间被消化了 | B. | 课外体育活动时,呼吸作用增强 | ||
| C. | 用生石灰作某些食品干燥剂 | D. | 水放进冰箱一段时间后结成冰 |
 下面关于水电解实验的叙述正确的是( )
下面关于水电解实验的叙述正确的是( )| A. | 水电解的化学方程式:2H2O=2H2↑+O2↑ | |
| B. | 实验说明水是由氢气和氧气组成的 | |
| C. | 实验说明水是由氢、氧两种元素组成的 | |
| D. | 若乙试管气体为5mL,则甲试管气体为10mL |
| A. | 苯胺是有机化合物 | B. | 苯胺分子中共有14个原子 | ||
| C. | 苯胺中C,N两种元素的质量比为6:1 | D. | 苯胺中氢原子的质量分数最大 |
| A. | 溶液中溶质的质量 | B. | 溶液的质量 | ||
| C. | 溶液中溶质的质量分数 | D. | 蔗糖的溶解度 |
| A. | 水结冰后形成的固体物质就是干冰 | |
| B. | 对天然水进行净化的各种处理中,净化程度最高的是蒸馏 | |
| C. | 市售的矿泉水清澈透明是纯净物 | |
| D. | 加明矾能使海水中的盐分沉淀而淡化 |
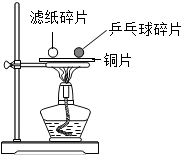 如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )| A. | 实验说明燃烧的条件之一是温度达到可燃物的着火点 | |
| B. | 铜片受热后变黑,可能是因为产生了氧化铜 | |
| C. | 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧 | |
| D. | 实验说明铜有导热性 |
