题目内容
13.如图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的实验装置图,试根据题目要求回答下列问题: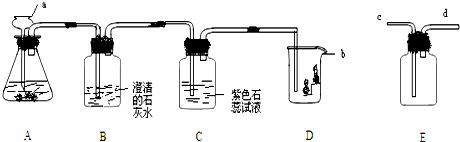
(1)仪器a的名称是长颈漏斗;装置B中发生的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.装置C中观察到的现象是石蕊试液变红色,写出装置A还可制取气体的反应方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(1)装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,可验证二氧化碳的性质是密度比空气大,不能燃烧,不支持燃烧.因此,二氧化碳可用于灭火.
(3)实验室用装置E来收集CO2时,CO2应从c端(填“c”或“d”)通入.
分析 (1)要熟悉各种仪器的名称、用途及其使用方法;考虑稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊,二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色.
(2)根据实验现象可以判断二氧化碳的性质,进一步可以判断二氧化碳有那些方面的用途.
(3)根据二氧化碳的密度可以判断收集二氧化碳的方法.
解答 解:(1)仪器a是长颈漏斗,通过长颈漏斗可以向锥形瓶中滴加液体;装置B可以用来检验CO2,发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O;装置A中,碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;装置C中二氧化碳进入石蕊试液中时,能和其中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色.
(2)因为二氧化碳的密度比空气大,不能燃烧,不支持燃烧,所以装置D中能够观察到下层蜡烛先熄灭,上层蜡烛后熄灭;二氧化碳在生活中可用于灭火.
(3)因为二氧化碳能溶于水,不能用排水法收集;因为二氧化碳的密度比空气大,可以用向上排空气法收集,实验室用装置E来收集二氧化碳时,二氧化碳应从c端通入.
故答案为:
(1)长颈漏斗; CO2+Ca(OH)2=CaCO3↓+H2O.石蕊试液变红色,CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)密度比空气大,不能燃烧,不支持燃烧. 灭火.(3)c.
点评 本题主要考查二氧化碳的制取、收集和性质,应该注意的是二氧化碳通入石蕊试液中时,石蕊试液变红色,不是二氧化碳能使石蕊试液变红色,而是二氧化碳和水反应生成的碳酸能使石蕊试液变红色.

练习册系列答案
相关题目
4.某金属制品厂清洗金属后产生一种黄色废液,小刚和小强欲对其成分进行探究.请你参与探究,填写空格:
【查阅资料】工业上通常使用稀盐酸或稀硫酸清洗金属表面的锈迹.
【猜想与假设】小刚认为废液中只含有硫酸铁;小强认为废液中可能还含有氯化铁.
【进行实验】小刚的实验报告如下:
【反思与改进】
(1)小强通过改进小刚的实验,证明了自己的猜想是正确的.小强的实验操作要点是:取少量澄清废液,先加入足量硝酸钡溶液,过滤,向滤液中滴加硝酸银溶液,产生白色沉淀.
(2)通过分析小刚的实验现象,简要说明他们探究过程中的不足之处:未考虑废液中含有酸.
【查阅资料】工业上通常使用稀盐酸或稀硫酸清洗金属表面的锈迹.
【猜想与假设】小刚认为废液中只含有硫酸铁;小强认为废液中可能还含有氯化铁.
【进行实验】小刚的实验报告如下:
| 实验步骤 | 实验现象 | 解释与结论 |
| ①取少量澄清废液于试管中,逐滴加入足量氢氧化钾溶液 | 刚开始没有明显现象,过一段时间后产生红褐色沉淀 | 生成红褐色沉淀的是氢氧化铁 |
| ②过滤,向滤液中滴加氯化钡溶液至恰好完全反应 | 产生白色沉淀 | 废液中一定含有硫酸铁 |
(1)小强通过改进小刚的实验,证明了自己的猜想是正确的.小强的实验操作要点是:取少量澄清废液,先加入足量硝酸钡溶液,过滤,向滤液中滴加硝酸银溶液,产生白色沉淀.
(2)通过分析小刚的实验现象,简要说明他们探究过程中的不足之处:未考虑废液中含有酸.
18.下列除去杂质的方法中,错误的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 通过足量的NaOH溶液、干燥 |
| D | FeSO4溶液(H2SO4) | 加入足量Fe粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.下列家庭小实验只发生物理变化的是( )
| A. |  用蜡烛燃烧生成炭黑的实验 | B. |  自制叶脉书签 | ||
| C. |  保鲜膜保鲜能力测试 | D. |  自制汽水 |


 下列字母A~H表不初中化中常见的物质,它们由氢、碳、氧、钠、钙、铁中的2-3种元素组成
下列字母A~H表不初中化中常见的物质,它们由氢、碳、氧、钠、钙、铁中的2-3种元素组成