题目内容
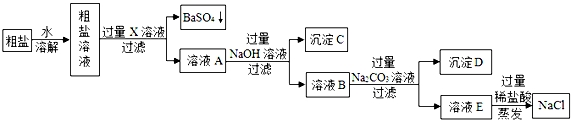
某固体混合物由K2CO3,K2SO4,CaCl2和KCl中的一种或几种组成,实验记录如下:
①取该样品溶于水,得到无色溶液;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀部分消失并产生气泡;
④取步骤②的溶液加入AgNO3溶液生成白色沉淀,再加入稀HNO3,振荡,沉淀不消失.
下列分析正确的是( )
A.原固体混合物中一定不含有CaCl2,KCl
B.原固体混合物中一定含有K2CO3,K2SO4,KCl
C.只通过步骤①②就可以确定原固体混合物中一定含有K2SO4
D.若步骤②改为滴加过量的Ba(NO3)2溶液,其余操作及现象均不变,则原固体混合物中一定含有KCl
【分析】根据物质的性质进行分析,碳酸钾能与氯化钙反应生成碳酸钙沉淀,硫酸钾与氯化钙结合能产生微溶于水的硫酸钙,形成沉淀;
①取该样品溶于水,得到无色溶液,说明碳酸钾、硫酸钾与氯化钙不能同时存在;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,说明含有碳酸钾或硫酸钾;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀部分消失并产生气泡,说明产生的沉淀一定有碳酸钡和硫酸钡;
④取步骤②的溶液加入AgNO3溶液生成白色沉淀,再加入稀HNO3,振荡,沉淀不消失,说明溶液中含有氯离子.
【解答】解:①取该样品溶于水,得到无色溶液,说明碳酸钾、硫酸钾与氯化钙不能同时存在;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,说明含有碳酸钾或硫酸钾,故原固体中一定不含有氯化钙;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀部分消失并产生气泡,说明产生的沉淀一定有碳酸钡和硫酸钡,说明原固体中一定含有碳酸钾和硫酸钾;
④取步骤②的溶液加入AgNO3溶液生成白色沉淀,再加入稀HNO3,振荡,沉淀不消失,说明溶液中含有氯离子,但是步骤②中加入了氯化钡,引入了氯离子,不能确定是否含有氯化钾;
A、原固体中不能确认是否含有氯化钾,故A错误;
B、原固体混合物中一定含有K2CO3,K2SO4,不一定含有KCl,故B错误;
C、通过实验①②不能说明一定含有硫酸钾,故C错误;
D、若步骤②改为滴加过量的Ba(NO3)2溶液,其余操作及现象均不变,则原固体混合物中一定含有KCl,故D正确;
故选D.

 阶梯计算系列答案
阶梯计算系列答案