题目内容
11. 在宏观、微观和符号之间建立联系是化学学科的特点.
在宏观、微观和符号之间建立联系是化学学科的特点.(1)萨罗(Salol)是一种消毒剂,其分子模型如图所示:该物质的一个分子中含有26个原子;萨罗(Salol)中氧元素的质量分数为22.4%.
(2)A、B、C、D表示4种物质,部分物质的微观示意图如表.A和B在一定条件下反应生成C和D.
| 物质 | B | C | D |  |
微观示意图 |  |  |  |
①A、B、C、D中属于单质的是B(填字母序号,下同);属于氧化物的是CD.
②A、B、C、D四种物质中由分子构成的是ABCD.
③若一定质量的A和4.8gB恰好完全反应,可生成4.4gC和2.7gD,则A中一定含有的元素是C、H、O,其化学式为C2H6O.
分析 (1)由分子模型图可知:该物质的分子构成;萨罗(Salol)中氢元素与氧元素的质量比.
(2)A、B、C、D表示4种物质,部分物质的微观示意图见下表.A和B在一定条件下反应生成C和D.
①由图可推测A中一定含有碳元素、氢元素,故为化合物,则可知A、B、C、D中属于单质的物质;属于氧化物的物质.
②根据在化学反应中元素质量守恒,则可计算A含有的元素.故可推测A的化学式.
解答 解:
(1)萨罗(Salol)是一种消毒剂,其分子模型如图可知:该物质的一个分子中含有26个原子;可推测:其化学式C13H10O3,萨罗(Salol)中氧元素的质量分数为$\frac{16×3}{13×12+10×1+16×3}×100%$=22.4%.
(2)A、B、C、D表示4种物质,部分物质的微观示意图见下表.A和B在一定条件下反应生成C和D.
请回答以下问题:
①根据质量守恒定律,可知A中的元素一定有氢元素、碳元素,则为化合物,则可推测A、B、C、D中属于单质的是B;根据氧化物概念:由两种元素组成,其中一种为氧元素,故可知属于氧化物的是CD.
②由四种物质的分子结构模拟图,4种物质均由分子构成;
③若一定质量的A和4.8g的B恰好完全反应,可生成4.4gC和2.7gD,4.4gC含有:氧元素的质量为4.4g×$\frac{32}{44}$×100%=3.2g,碳元素的质量为4.4-3.2=1.2克;2.7gD含有:氧元素的质量为2.7g×$\frac{16}{18}$×100%=2.4g,则氢元素2.7g-2.4g=0.3g,因为B的质量为4.8g,小于C、D中氧元素的质量;故A中含有氧元素的质量是:3.2g+2.4g-4.8g=0.8g故A中含有碳、氢、氧元素,则其原子个数比为:$\frac{1.2g}{12}:\frac{0.3g}{1}:\frac{0.8g}{16}$=2:6:1,故A的化学式为C2H6O.
故答为:(1)26;22.4%.(2)①B; C、D.②ABCD;③C、H、O;C2H6O.
点评 通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力;以检测考生从微观角度认识化学的意识和能力.

| A. | CO2分子是由一个碳原子和一个氧分子构成 | |
| B. | 不同元素的原子核电荷数一定不同 | |
| C. | 核外电子排布相同的粒子一定属于同种元素 | |
| D. | 原子、分子、元素都可构成物质 |
| A. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 切完西瓜的菜刀洗净擦干放在通风干燥处可以防止生锈 | |
| C. | 用黄铜片(铜锌合金)和铜片相互刻画,黄铜片上留有划痕 | |
| D. | 将二氧化碳通入燃着的两支高低蜡烛的烧杯中,蜡烛自低到高依次熄灭 |
【提出问题】一定金属与盐酸反应快慢受哪些因素的影响呢?
【猜想与假设】a.可能与盐酸的浓度有关;b.可能与反应时的温度有关.
【设计并进行实验】小明用不同质量分数的盐酸和相同形状的铝片进行如下实验.
| 实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 收集40mL气体所需时间/s |
| ① | 5% | 30 | 48 |
| ② | 10% | 20 | 41 |
| ③ | 5% | 20 | 69 |
| ④ | 10% | 30 | 32 |
(1)写出铝与盐酸反应的化学方程式2Al+6HCl=2AlCl3+3H2↑.
(2)通过实验②③对比,说明其他条件相同时,盐酸的浓度越大,反应速率越快;通过实验①③或②④(写编号)对比,说明反应时的温度对反应快慢有影响.
(3)如果盐酸的浓度为10%,温度为25℃,则收集40mL气体所需的时间范围为32s<t<41s.
(4)小明在做以上四组实验时,发现一开始反应速率都很慢,原因是铝片可能没有打磨,实验前没有除去铝表面的氧化膜.
(5)还有哪些因素会影响金属与酸的反应快慢金属的形状(或金属的纯度或反应物的量).

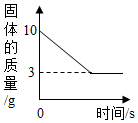 某同学取Fe粉与Cu粉混合物样品,加入足量的稀盐酸,待反应完全后过滤,称得固体质量如图所示,试计算:
某同学取Fe粉与Cu粉混合物样品,加入足量的稀盐酸,待反应完全后过滤,称得固体质量如图所示,试计算: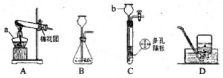 结合图示实验装置,回答下列问题.
结合图示实验装置,回答下列问题. 溶液是一类重要的混合物,具有广泛用途.
溶液是一类重要的混合物,具有广泛用途.