题目内容
20.如图,某电镀厂排放的污水中含有CuSO4、FeSO4和ZnSO4,为减少水污染及节约成本,回收重要物质硫酸锌、金属铁和铜,设计如图流程.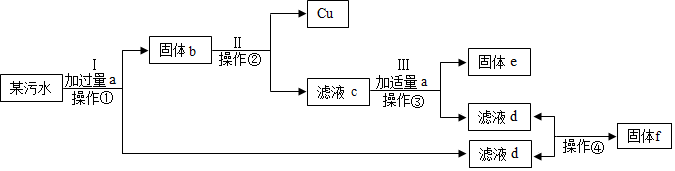
(1)固体b的成分是锌、铁、铜(填名称)
(2)上述流程的四个操作中,有一个和其他三个不同,它是④
(3)制作过滤器时滤纸润湿后应紧贴漏斗,不留气泡,若留有气泡后果是过滤速度太慢
(4)过程II中可以加入的物质有两种,它们是稀硫酸和硫酸铜,过程III中一定发生的化学方程式是Zn+FeSO4=ZnSO4+Fe
(5)上述物质中含有锌元素的是abcdf(填字母)
分析 可以根据物质之间相互作用时能否发生反应及其反应时生成物是什么等方面进行分析、考虑,从而得出正确的结论,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:因为锌比铜和铁活泼,所以能把硫酸铜、硫酸亚铁中的铜、铁置换出来.锌能和稀硫酸反应生成硫酸锌,铁能与稀硫酸反应生成硫酸亚铁,铜不能和稀硫酸反应,从而把铜分离出来.硫酸锌溶液经过蒸发得到硫酸锌固体.
(1)为减少水污染及节约成本,回收重要物质硫酸锌、金属铁和铜,因此污水中首先加入过量的锌粉,锌比铜和铁活泼,所以能把硫酸铜、硫酸亚铁中的铜、铁置换出来,因此固体b中含有锌、铁和铜,故填:锌、铁、铜;
(2)操作①②③都是将固体和液体分离的操作,都是过滤,操作④将液体中的水分蒸发,是蒸发结晶,故填:④;
(3)制作过滤器时滤纸润湿后应紧贴漏斗,不留气泡,若留有气泡后果是过滤速度太慢,故填:过滤速度太慢;
(4)要分离出铜,可以加入稀硫酸或是硫酸铜溶液的方法,得到的滤液中含有硫酸亚铁和硫酸锌,要分离出硫酸锌和铁,可以加入金属锌,锌能与硫酸亚铁反应生成硫酸锌和铁,故填:稀硫酸或是硫酸铜,Zn+FeSO4=ZnSO4+Fe.
(4)为减少水污染及节约成本,回收重要物质硫酸锌、金属铁和铜,因此污水中首先加入过量的锌粉,因此a是锌,b中含有过量的锌和置换出的铁、铜,Ⅱ中加硫酸或硫酸铜,锌、铁硫酸或硫酸铜,因此与c中含有硫酸亚铁和过量的硫酸锌,Ⅲ是加过量的铁粉,因此d中含有硫酸锌,e中含有的是铁,f 是硫酸锌固体,故填:abcdf.
点评 本题考查的是金属的性质,完成此题,可以依据已有的金属活动性顺序的意义进行.

练习册系列答案
相关题目
11.化学方程式中“═”的意义包括( )
①反应物、生成物的元素种类相同
②反应物、生成物的质量总和相等
③反应物、生成物中原子种类相同
④反应物、生成物中原子数目相等
⑤反应物、生成物中分子数目相等
⑥反应物、生成物的体积相等
⑦“生成”的意思.
①反应物、生成物的元素种类相同
②反应物、生成物的质量总和相等
③反应物、生成物中原子种类相同
④反应物、生成物中原子数目相等
⑤反应物、生成物中分子数目相等
⑥反应物、生成物的体积相等
⑦“生成”的意思.
| A. | ②⑦ | B. | ①③⑤⑦ | C. | ②④⑥⑦ | D. | ①②③④⑦ |
8.下列关于淀粉的说法不正确的是( )
| A. | 淀粉与葡萄糖组成元素相同,属于同一物质 | |
| B. | 淀粉属于高分子化合物 | |
| C. | 淀粉是由碳、氢、氧组成的有机化合物 | |
| D. | 淀粉与碘作用呈蓝色 |
15.下列物质不属于空气污染物的是( )
| A. | 飘尘 | B. | 二氧化硫 | C. | 二氧化碳 | D. | 二氧化氮 |
5.铁生锈的变化是( )
| A. | 燃烧 | B. | 缓慢氧化 | C. | 自燃 | D. | 置换反应 |
12.下列关于铁的做法或说法错误的是( )
| A. | 铁钉在潮湿的空气中易生锈 | |
| B. | 铁和稀盐酸反应生成氯化亚铁和氢气 | |
| C. | 用铁桶盛放硫酸铜溶液 | |
| D. | 炼铁高炉内一氧化碳夺取氧化铁中的氧而生成了铁和二氧化碳 |
9. 为探究催化剂对双氧水(H2O2)分解的催化效果,其研究小组做了如下实验:
为探究催化剂对双氧水(H2O2)分解的催化效果,其研究小组做了如下实验:
实验一:图中的实验能否证明MnO2是双氧水分解反应的催化剂?并说明理由不能;因为没有确认MnO2的质量和性质是否改变.
数据记录表
实验二:从从表格的设计可以看出,该实验的目的是MnO2质量的多少对H2O2分解的速率是否有影响.
 为探究催化剂对双氧水(H2O2)分解的催化效果,其研究小组做了如下实验:
为探究催化剂对双氧水(H2O2)分解的催化效果,其研究小组做了如下实验:实验一:图中的实验能否证明MnO2是双氧水分解反应的催化剂?并说明理由不能;因为没有确认MnO2的质量和性质是否改变.
数据记录表
| 1%H2O2溶液(mL) | 50 | 50 | 50 |
| 加入MnO2的质量(g) | 0.1 | 0.2 | 0.4 |
| 测量40秒末得到O2体积(mL) |
10.在下列某种气体的性质中,属于化学性质的是( )
| A. | 常温下为无色气体 | B. | 难溶于水 | ||
| C. | 没有气味 | D. | 可以燃烧 |