题目内容
某实验小组同学用12.0克氯酸钾和二氧化锰的混合物来制取氧气,反应完全后在相同条件下称得剩余固体的质量为8.16克.试计算:
(1)该小组同学共制得氧气多少克?
(2)消耗氯酸钾多少克?
(1)该小组同学共制得氧气多少克?
(2)消耗氯酸钾多少克?
(1)根据质量守恒定律,生成氧气的质量=12.0g-8.16g=3.84g
(2)设消耗氯酸钾的质量为x,
2KClO3
2KCl+3O2↑
245 96
x 3.84g
=
x=9.80g
答:消耗氯酸钾9.80g.
(1)3.84g;
(2)9.80 g.
(2)设消耗氯酸钾的质量为x,
2KClO3
| ||
| △ |
245 96
x 3.84g
| 245 |
| x |
| 96 |
| 3.84g |
x=9.80g
答:消耗氯酸钾9.80g.
(1)3.84g;
(2)9.80 g.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
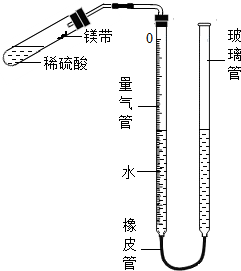 某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是: