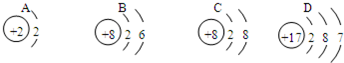题目内容
过氧化氢在二氧化锰的催化作用下分解,生成水和氧气.若把过氧化氢水溶液、二氧化锰、氧化钙、氯化镁混合后,发生的反应均不属于下列基本反应类型中的( )
| A、化合反应 | B、分解反应 | C、置换反应 | D、复分解反应 |
分析:由题意“把过氧化氢水溶液、二氧化锰、氧化钙、氯化镁混合”,则会发生反应:过氧化氢在二氧化锰的作用下分解出水和氧气;氧化钙与水反应生成氢氧化钙;氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙.
再根据:化合反应的特点:“多变一”即两种或两种以上的物质生成一种物质的反应.分解反应的特点:“一变多”是指一种物质生成多种物质的反应.置换反应是指一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应;复分解反应是指两种化合物相互交换成分生成另外两种化合物的反应;则可知答案.
再根据:化合反应的特点:“多变一”即两种或两种以上的物质生成一种物质的反应.分解反应的特点:“一变多”是指一种物质生成多种物质的反应.置换反应是指一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应;复分解反应是指两种化合物相互交换成分生成另外两种化合物的反应;则可知答案.
解答:解:过氧化氢在二氧化锰的作用下分解出水和氧气,该反应符合“一变多”,为分解反应;氧化钙与水反应生成氢氧化钙,该反应符合“多变一”,为化合反应;氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,该反应符合复分解反应的概念,为复分解反应,则可知无置换反应.
故选:C.
故选:C.
点评:掌握四大基本反应类型的判定方法;了解物质的性质及其发生的反应,培养了学生分析问题解决问题的能力.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
某课外活动小组加热氧化铜和炭粉(过量)的混合物,得到的铜粉中含有炭粉,他们用下图所示的装置,对获得的铜粉样品进行实验分析.以测定样品中铜的质量分数.(图中铁架台等装置已略去.)已知,过氧化氢在二氧化锰的催化作用下分解产生氧气.请你帮他们完成实验报告.
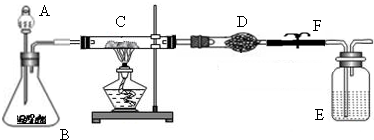
(1)实验过程:
(2)计算:
样品中铜的质量分数= (用含w、m1、m2的代数式表示)
(3)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果.经时论,有同学提出在B与C之间加入一个装置.再次实验后.得到了较正确的结果,那么,原来实验所测得的铜的质量分数偏小的原因可能是在B与C之间加入的装置可以是 ;其中盛放的药品是 .

(1)实验过程:
| 编号 | 实验步骤 | 实验现象 | 有关化学方程式 |
| a | 连接好仪器后,打开止水夹F.检查 气密性(观察).在C中加入样品粉末 Wg,在D中装入药品后称量为m1g |
||
| b | 打开A的活塞,慢慢滴加溶液 | ||
| c | 对C进行加热当C中药品充分反应 后,关闭A的活塞、关F,停止加热 |
||
| d | 冷却后,称得D的质量为m2g |
样品中铜的质量分数=
(3)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果.经时论,有同学提出在B与C之间加入一个装置.再次实验后.得到了较正确的结果,那么,原来实验所测得的铜的质量分数偏小的原因可能是在B与C之间加入的装置可以是
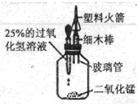 22、某学生利用上述原理设计了如图所示的装置,表演趣味化学实验--“发射火箭”.表演时,挤压胶头滴管时:观察到的现象是
22、某学生利用上述原理设计了如图所示的装置,表演趣味化学实验--“发射火箭”.表演时,挤压胶头滴管时:观察到的现象是