题目内容
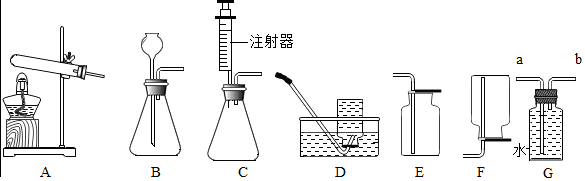
6.某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下几组实验,请你参与并回答下列问题.
(1)在实验A中,刚接通电源时观察到的现象是两电极上产生气泡;
(2)在实验B中,使用过量的白磷的目的是将空气中的氧气耗尽;
(3)实验C中集气瓶底预留少量水的作用是防止生成物融化,溅落下来炸裂集气瓶.
分析 (1)根据电解水实验的现象及结论进行分析解答;
(2)根据使用过量的白磷的目的是将空气中的氧气耗尽解答;
(3)根据铁在氧气中燃烧的注意事项解答.
解答 解:
(1)在实验A中,刚接通电源时观察到的现象是两电极上产生气泡;
(2)在实验B中,使用过量的白磷的目的是将空气中的氧气耗尽;
(3)实验C中集气瓶底预留少量水的作用是防止生成物融化,溅落下来炸裂集气瓶.
答案:
(1)两电极上产生气泡;
(2)将空气中的氧气耗尽;
(3)防止生成物融化,溅落下来炸裂集气瓶.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
16.实验室提供下列药品:Na2CO3固体、CaCO3固体、稀H2SO4、稀HCl、和浓HCl;A、B、C、D、E、F、G、H等装置和试管等仪器.(用字母序号填空):

(1)制取CO2的发生装置选B,按要求连接好装置后,在装入药品之前必不可少的操作是检查装置气密性.制CO2的装置还可以用来制取氧气或氢气气体,其反应原理是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(Zn+H2SO4=ZnSO4+H2↑)(用化学方程式表示).
(2)检验二氧化碳的方法用化学方程式表示为CO2+Ca(OH)2=CaCO3↓+H2O.
(3)在四支试管中取等量固体和稀硫酸、稀盐酸反应,现象如下表,由此推知,实验室用于制取CO2的药品最合理的是③(填序号);反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,
(4)若要制取干燥的CO2,所有装置的连接顺序为BCG;
(5)若不慎用浓盐酸代替稀盐酸制得了CO2气体,要得到纯净干燥的CO2,所有装置的连接顺序为BECG.

(1)制取CO2的发生装置选B,按要求连接好装置后,在装入药品之前必不可少的操作是检查装置气密性.制CO2的装置还可以用来制取氧气或氢气气体,其反应原理是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(Zn+H2SO4=ZnSO4+H2↑)(用化学方程式表示).
(2)检验二氧化碳的方法用化学方程式表示为CO2+Ca(OH)2=CaCO3↓+H2O.
(3)在四支试管中取等量固体和稀硫酸、稀盐酸反应,现象如下表,由此推知,实验室用于制取CO2的药品最合理的是③(填序号);反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,
| 反应物 | ①碳酸钙粉末+稀盐酸 | ②碳酸钠+稀硫酸 | ③块状碳酸钙+稀盐酸 | ④碳酸钙+稀硫酸 |
| 现 象 | 剧烈,瞬间完成 | 剧烈,瞬间完成 | 有平稳气流产生 | 很慢,稍后停止 |
(5)若不慎用浓盐酸代替稀盐酸制得了CO2气体,要得到纯净干燥的CO2,所有装置的连接顺序为BECG.
14.除去下列物质中含有的杂质,选用的试剂和操作都正确的是( )
| 序号 | 物质 | 杂质 | 选用试剂和操作 |
| A | CaCO3粉末 | Na2CO3 | 溶于水、过滤、洗涤、干燥 |
| H | KCl溶液 | K2CO3 | 加入过量盐酸、搅拌 |
| C | Cu | Fe | 加入过量稀硫酸、过滤、洗涤、干燥 |
| D | FeCl2 | CuCl2 | 加入过量的锌粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.如表列出了 20℃时NaCl溶解实验的一组数据.
以上实验组中,得到的溶液属于饱和溶液的是③④(填序号),由如表的数据可知在20℃时,NaCl溶解度为36g.
| 实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
| ① | 100 | 20 | 120 |
| ② | 100 | 30 | 130 |
| ③ | 100 | 36 | 136 |
| ④ | 100 | 40 | 136 |