题目内容
豆浆被称为“植物奶”,其中含有异黄酮(C15H20O2)。据此请计算:
(1)异黄酮中碳、氢、氧三种元素的原子个数比为 ;
(2)异黄酮中氢、氧元素的质量比 ;
(3)232g异黄酮中碳元素的质量为 g。
【答案】
(1)15:20:2;(2)20:32(或5:8);(3)180。
【解析】
试题分析:(1)分子是由原子构成的,根据异黄酮(C15H10O2)化学式可知,一个异黄铜分子中含有15个碳原子、20个氢原子和两个氧原子,故碳、氢、氧三种元素的原子个数比15:20:2 ;(2)异黄酮中氢、氧元素的质量比为(1×20):(16×2)=20:32(或5:8);(3)232g异黄酮中碳元素的质量为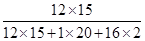 ×232=180
×232=180
考点:化学式的书写及意义;元素质量比的计算;元素的质量分数计算.

练习册系列答案
相关题目
豆浆被称为“植物奶”,其中含有的异黄酮(C15H10O2)具有防癌功能.下列根据异黄酮的化学式进行的计算正确的是( )
| A、异黄酮的相对分子质量:Mr(C15H10O2)=12g×15+1g×10+16g×2=222g | ||
| B、异黄酮中C、H、O三种元素的质量比为15:10:2 | ||
C、异黄酮中碳元素的质量分数:ω(C)=
| ||
| D、1个异黄酮分子中共含有27个原子 |