题目内容
7.下列物质属于氧化物的是( )| A. | Ca(OH)2 | B. | CO2 | C. | CH4 | D. | H2SO4 |
分析 物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,CO2属于氧化物.
解答 解:A、Ca(OH)2属于纯净物中的化合物,故选项错误;
B、氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,CO2属于氧化物,故选项正确;
C、CH4属于纯净物中的化合物,故选项错误;
D、H2SO4属于纯净物中的化合物,故选项错误;
故选B
点评 本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
10.在一定条件下,同一反应进行的快慢与反应物的溶质质量分数成正比.现在用100克溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点而又不影响生成氢气的总量,可以向该硫酸溶液中加入适量的( )
| A. | 氢氧化钠 | B. | 硫酸钾溶液 | C. | 碳酸钠溶液 | D. | 碱式碳酸铜 |
11.甲、乙的溶解度曲线如图所示.下列有关说法不正确的是( )


| A. | t2℃时,甲的饱和溶液中溶质和溶剂的质量之比为2:5 | |
| B. | 乙的饱和溶液从t2℃降温到t1℃,溶液仍饱和 | |
| C. | t1℃时,甲、乙两种饱和溶液中溶质的质量相等 | |
| D. | 甲、乙两种饱和溶液分别从t2℃降温到t1℃,两溶液中溶质质量分数相等 |
8.下列图象能正确反映其对应关系的是( )
| A. |  向等质量的铁粉和锌粉中分别加入过量的稀硫酸 | |
| B. |  向一定量KNO3的不饱和溶液中不断加入KNO3固体 | |
| C. |  等质量的镁和氧气在点燃条件下充分反应 | |
| D. |  过氧化氢溶液与二氧化锰混合 |
2.甲组同学往20克10%的氢氧化钠溶液样品中滴加10% 的盐酸(室温下).如图描述的是氢氧化钠与盐酸反应的微观实质.
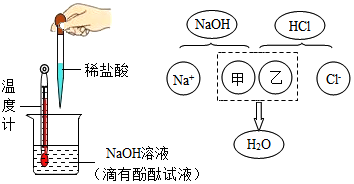
(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
(3)从能量角度
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)

(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度上升(△t)/℃ | 5.6 | 12.1 | 18.5 | 15.2 | 13.5 |
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)
16.下列说法正确的是( )
| A. | 由同种元素组成的物质是单质,由不同种元素组成的物质是化合物 | |
| B. | 水银是化合物,水是单质 | |
| C. | 空气是由几种单质和几种化合物组成的混合物 | |
| D. | 二氧化碳是由碳和氧气两种单质组成的 |
17.不需其他试剂就能区别的一组溶液是( )
| A. | FeCl3 NaOH KCl Ba(NO3)2 | |
| B. | NaCl Na2CO3 KNO3 HCl | |
| C. | Na2SO4 BaCl2 K2CO3 KNO3 | |
| D. | BaCl2 CuSO4 NaOH NaCl |

