题目内容
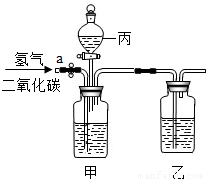 有稀盐酸、浓硫酸和氢氧化钠溶液.要用如图所示装置对H2和CO2的混合气体进行分离和干燥,则:
有稀盐酸、浓硫酸和氢氧化钠溶液.要用如图所示装置对H2和CO2的混合气体进行分离和干燥,则:(1)甲中应盛放______;乙中应盛放______;
(2)首先打开活塞a,可分离出______;反应的化学方程式为______;
(3)再关闭活塞a,从漏斗丙加入______又可以分离出______,反应的化学方程式为______.
【答案】分析:(1)整个实验操作流程是:甲中盛放NaOH溶液,用来吸收CO2,乙中盛放浓硫酸,用来干燥H2,此时H2已分离出来;然后把丙中的稀盐酸滴入甲中,这时被吸收的CO2又重新释放出来,被乙中的浓硫酸干燥.
(2)打开活塞a,关闭活塞b,二氧化碳被吸收,可分离出H2,根据二氧化碳和氢氧化钠溶液反应书写化学方程式;
(3)关闭a,打开b,盐酸和碳酸钠反应,生成二氧化碳气体.
解答:解:(1)甲中装有NaOH溶液,用来吸收CO2,此时从乙中出来的是被乙中浓硫酸干燥过的纯净的H2,因为该题中要求分离H2和CO2,所以最终还要求把甲中吸收的CO2再放出来,所以丙中装稀盐酸,用来生成CO2;
(2)若关闭活塞b,打开活塞a,可分离出 H2,反应的化学方程式为 CO2+2NaOH=Na2CO3↓+H2O.
(3)若关闭活塞a,打开活塞b,又可分离出 CO2,反应的化学方程式为 Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)甲:NaOH溶液乙:浓硫酸
(2)H2、CO2+2NaOH═Na2CO3+H2O
(3)稀盐酸;CO2;2HCl+Na2CO3═2NaCl+H2O+CO2↑
点评:此题考查了H2与CO2的分离方式,实际上是先通过试剂除掉一种物质,而后再把吸收后的物质与其他物质反应制取出开始除掉的物质.
(2)打开活塞a,关闭活塞b,二氧化碳被吸收,可分离出H2,根据二氧化碳和氢氧化钠溶液反应书写化学方程式;
(3)关闭a,打开b,盐酸和碳酸钠反应,生成二氧化碳气体.
解答:解:(1)甲中装有NaOH溶液,用来吸收CO2,此时从乙中出来的是被乙中浓硫酸干燥过的纯净的H2,因为该题中要求分离H2和CO2,所以最终还要求把甲中吸收的CO2再放出来,所以丙中装稀盐酸,用来生成CO2;
(2)若关闭活塞b,打开活塞a,可分离出 H2,反应的化学方程式为 CO2+2NaOH=Na2CO3↓+H2O.
(3)若关闭活塞a,打开活塞b,又可分离出 CO2,反应的化学方程式为 Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)甲:NaOH溶液乙:浓硫酸
(2)H2、CO2+2NaOH═Na2CO3+H2O
(3)稀盐酸;CO2;2HCl+Na2CO3═2NaCl+H2O+CO2↑
点评:此题考查了H2与CO2的分离方式,实际上是先通过试剂除掉一种物质,而后再把吸收后的物质与其他物质反应制取出开始除掉的物质.

练习册系列答案
相关题目