题目内容
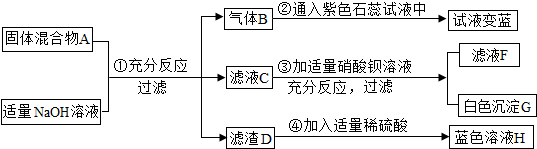
19.硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).查阅资料发现常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).
根据以上信息,回答下列问题:
(1)固体A的成分为Si、C,滤液B中的金属阳离子为Fe2+;
(2)写出步骤⑦中发生反应的化学方程式3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;其基本反应类型为置换反应;
(3)在过滤操作时,若发现滤液浑浊,应再过滤一次;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 (1)根据硅钢成分以及与盐酸反应情况解答;
(2)碳还原氧化铁生成铁和二氧化碳写化学方程式,判断反应类型;
(3)根据过滤的操作分析;
(4)根据Fe(OH)2在空气中与氧气和水反应写化学方程式.
解答 解:(1)硅钢中主要含有Fe、C、Si,只有Fe能与稀盐酸反应生成氯化亚铁,故剩余的固体A的成分中含有C、Si,滤液B中的金属阳离子为Fe2+;
(2)碳还原氧化铁生成铁和二氧化碳,反应的化学方程式为3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;
(3)过滤后发现滤液仍浑浊,先查找原因后根据原因调整改进后再重新过滤;
(4)反应物是Fe(OH)2与氧气和水,写在等号的左边,生成物是氢氧化铁写在等号的右边,用观察法配平即可,所以方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故答案为:
(1)C、Si;Fe2+;
(2)3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑;置换反应;
(3)再过滤一次;
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
点评 解答本题关键是要知道回收金属时,是利用排在盐中金属元素前面的金属把盐中的金属元素置换出来,为了反应完全,要加入过量的金属,固体中会混有置换出来的金属和过量的金属,再利用二者性质的不同进行分离.

练习册系列答案
相关题目
14.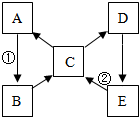 A.B.C.D.E是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:五种物质均含有铜元素,且化合物中的化合价均为+2价;A为单质,在空气中加热生成黑色物质B; C溶液与铁反应可得A;C溶液与氯化钡溶液反应得D,同时又白色沉淀生成;D溶液中加入氢氧化钠溶液得到E.结合信息判断下列叙述正确的是( )
A.B.C.D.E是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:五种物质均含有铜元素,且化合物中的化合价均为+2价;A为单质,在空气中加热生成黑色物质B; C溶液与铁反应可得A;C溶液与氯化钡溶液反应得D,同时又白色沉淀生成;D溶液中加入氢氧化钠溶液得到E.结合信息判断下列叙述正确的是( )
 A.B.C.D.E是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:五种物质均含有铜元素,且化合物中的化合价均为+2价;A为单质,在空气中加热生成黑色物质B; C溶液与铁反应可得A;C溶液与氯化钡溶液反应得D,同时又白色沉淀生成;D溶液中加入氢氧化钠溶液得到E.结合信息判断下列叙述正确的是( )
A.B.C.D.E是初中化学常见的物质,各物质之间的相互转化的关系如图所示(部分反应物、生成物及条件略去).已知:五种物质均含有铜元素,且化合物中的化合价均为+2价;A为单质,在空气中加热生成黑色物质B; C溶液与铁反应可得A;C溶液与氯化钡溶液反应得D,同时又白色沉淀生成;D溶液中加入氢氧化钠溶液得到E.结合信息判断下列叙述正确的是( )| A. | ①反应是吸热反应 | B. | C溶液是无色透明的液体 | ||
| C. | ②反应中和反应 | D. | C、D、E均是盐类 |
8.在化学反应6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$C6H12O6+6O2中没有涉及到的物质类别是( )
| A. | 单质 | B. | 氧化物 | C. | 盐 | D. | 有机化合物 |
9.坚持绿色发展,构建生态盐城,下列做法不符合这一宗旨的是( )
| A. | 扩大公共绿地,打造绿色家园 | B. | 鼓励燃煤发电,保障电力供应 | ||
| C. | 禁止秸杆燃烧,减轻雾霾影响 | D. | 发展公共交通,提倡低碳生活 |
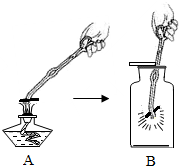 今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答:
今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答: