题目内容
15.CO2和CO的混合气体5g与足量灼热的氧化铁充分反应后,将生成的气体全部通入80克质量分数为20%的氢氧化钠溶液中充分吸收,测得最终所得溶液的质量为86.6克,则原混合气体中碳元素和氧元素的质量比为( )| A. | 9:16 | B. | 1:2 | C. | 3:8 | D. | 17:8 |
分析 根据一氧化碳会与氧化铁反应生成二氧化碳,通过分析可知反应后氢氧化钠溶液增加的质量即为二氧化碳质量,二氧化碳中碳元素的质量即为混合气体中碳元素质量.
解答 解:通过分析可知,混合气中的一氧化碳会与氧化铁中的氧元素生成二氧化碳,通过分析可知反应后氢氧化钠溶液增加的质量即为二氧化碳质量,氢氧化钠溶液增加的质量为:86.6g-80g=6.6g.
二氧化碳中碳元素的质量即为混合气体中碳元素质量.混合气体中碳元素质量:6.6g×$\frac{12}{44}$=1.8g,混合气体中氧元素的质量为5g-1.8g=3.2g;
混合气体中碳元素和氧元素的质量比为:1.8g:3.2g=9:16;
答案:A.
点评 根据反应前后气体物质的质量变化,利用化学方程式的气体差量进行参加反应气体的计算,可使复杂的计算得以简化.

练习册系列答案
相关题目
5.下列化学方程式与实际相符,且书写正确的是( )
| A. | 酸雨形成原因:CO2+H2O=H2CO3 | |
| B. | CO2通入CaCl2溶液中:CO2+CaCl2+H2O=CaCO3↓+2HCl | |
| C. | 用稀盐酸除去铁锈的原理:6HCl+Fe2O3=2FeCl2+3 H2O | |
| D. | 医疗上用碳酸氢钠治疗胃酸过多:NaHCO3+HCl=NaCl+H2O+CO2↑ |
10.某粒子的结构示意图如图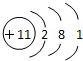 所示,下列对该粒子的判断中,错误的是( )
所示,下列对该粒子的判断中,错误的是( )
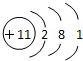 所示,下列对该粒子的判断中,错误的是( )
所示,下列对该粒子的判断中,错误的是( )| A. | 原子核内有11个质子 | B. | 该粒子是钠原子 | ||
| C. | 该元素的一个离子含有11个电子 | D. | 该元素在化合物中显+1价 |
7.对下面符号的理解,正确的是( )
| A. | Fe2+中的“2”表示一个铁离子带两个单位的正电荷 | |
| B. | NO2、N2O4中氮元素的化合价都是+4价,是同一化合物 | |
| C. | NH4NO3中氮元素有两种不同的化合价 | |
| D. | P2O5中的“5”表示五氧化二磷中有5个氧原子 |
4.下列有关物质的鉴别、检验、除杂所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别氯化钠溶液和稀盐酸 | 无色酚酞 |
| B | 鉴别硫酸钠溶液和硝酸钾溶液 | 氯化钡溶液 |
| C | 除去氧化钙中的少量碳酸钙 | 加水溶解后过滤 |
| D | 除去二氧化碳中的HCl | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |

