题目内容
12.生活中处处有化学,化学与生活密切相关.(1)山药中含有碱性皂角素,皮肤沾上会奇瘁难忍.可涂厨房中的食醋来止痒.
(2)铁元素是人体必需的一种微量元素.食用“加铁酱油”可预防贫血.
(3)小明把划着的火柴放到嘴里,迅速合上嘴.他没被烧伤原因是隔绝了氧气.
(4)无人驾驶汽车处理系统的核心材料是高纯度的硅.工业制硅的反应之一如下:
2X+SiCl4═Si+4HCl.该反应中,x的化学式是H2.
分析 (1)根据酸和碱能发生中和反应进行分析解答;
(2)根据铁的生理功能和缺乏症进行分析解答;
(3)根据燃烧的条件来分析;
(4)根据化学反应前后,原子种类和数目不变来分析.
解答 解:(1)食醋呈酸性,可以与碱性物质反应,故填:食醋;
(2)铁元素是人体必需的一种微量元素.铁是合成血红蛋白的主要元素,缺乏会患贫血,食用“加铁酱油”可预防缺铁性贫血.故填:贫血;
(3)把划着的火柴放到嘴里,迅速合上嘴,由于没有氧气所以火迅速熄灭而没有烧伤;故填:隔绝了氧气;
(5)反应前:1个硅原子,4个氯原子;反应后:1个硅原子、4个氯原子和4个氢原子,因此2X中含有4个氢原子,故X的化学式为H2;故填:H2.
点评 本题难度不大,掌握酸碱中和的原理、化学元素与人体健康的关系、灭火的原理以及质量守恒定律及其应用是正确解答此类题的关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
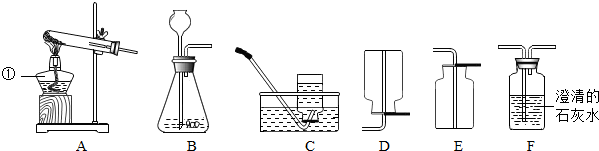
2.根据下列实验装置图,回答问题:
(1)写出图中标号仪器名称:a酒精灯、b长颈漏斗;
(2)实验室中若用装置A制取氧气,化学反应方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若要收集一瓶较纯净的氧气,应选用的收集装置为C(填字母),若用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;
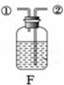
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的发生装置和收集装置的组合为BD(填字母),检验二氧化碳是否集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口(填“①”或“②”)通入.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室中若用装置A制取氧气,化学反应方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若要收集一瓶较纯净的氧气,应选用的收集装置为C(填字母),若用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的发生装置和收集装置的组合为BD(填字母),检验二氧化碳是否集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口(填“①”或“②”)通入.
3.氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
| A. | 向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失 | |
| B. | 在NaAlO2中铝元素的化合价为+3价 | |
| C. | 向稀盐酸中加入氢氧化铝,发生中和反应 | |
| D. | 氢氧化铝属于氧化物 |
20.实验室制取气体所需装置如图1所示.
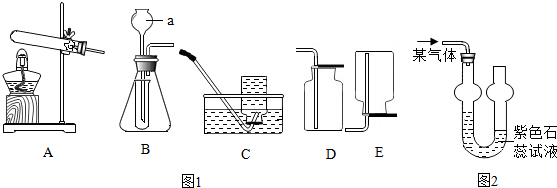
请回答以下问题:
(1)写出仪器a的名称:长颈漏斗;
(2)B中小试管的作用:液封或节约药品或可控制反应;
(3)甲烷是一种无色无味的气体,难溶于水,密度比空气小且不与空气反应.用加热无水醋酸钠和碱石灰的固体混合物制取较纯净的甲烷,应选择的制取装置是AC;
(4)双球洗气管常用于气体除杂、干燥、吸收(可防倒吸)等实验.为吸收某气体并检验其性质进行图2中实验,发现紫色石蕊试液变色.请根据表中的数据判断左方进入的气体可能是BC(填字母).
A.O2 B.HCl C.NH3 D.CO2.

请回答以下问题:
(1)写出仪器a的名称:长颈漏斗;
(2)B中小试管的作用:液封或节约药品或可控制反应;
(3)甲烷是一种无色无味的气体,难溶于水,密度比空气小且不与空气反应.用加热无水醋酸钠和碱石灰的固体混合物制取较纯净的甲烷,应选择的制取装置是AC;
(4)双球洗气管常用于气体除杂、干燥、吸收(可防倒吸)等实验.为吸收某气体并检验其性质进行图2中实验,发现紫色石蕊试液变色.请根据表中的数据判断左方进入的气体可能是BC(填字母).
| O2 | HCl | NH3 | CO2 | |
| 通常情况下,1体积水 能吸收的气体的体积 | 0.031 | 500 | 700 | 1 |
7.在中考体育考试中,很多学生在测试结束后感觉小腿酸痛,这是因为在剧烈的高强度运动中,人体内的葡萄糖(C6H1206)会进行无氧反应,产生乳酸(C3H603),下列说法正确的是( )
| A. | 乳酸是一种氧化物 | |
| B. | 乳酸分子是山碳元素、氢元素和氧元素组成的 | |
| C. | 葡萄糖与乳酸中所含的元素种类相同 | |
| D. | 葡萄糖不能为人体提供能量 |
17.根据如图五种粒子的结构示意图,所获取的信息正确的是( )
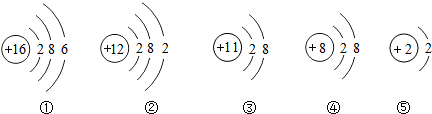
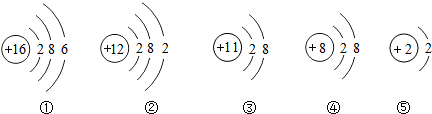
| A. | ①②属于第三周期元素,③④属于第二周期元素 | |
| B. | ③④、②⑤的化学性质相似 | |
| C. | ①元素最高正价为+6价,负价为-2价 | |
| D. | ①②表示的是原子,而③④⑤表示的是阴离子 |
1.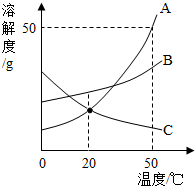 如图是A、B、C三种物质的曲线,下列分析正确的是( )
如图是A、B、C三种物质的曲线,下列分析正确的是( )
 如图是A、B、C三种物质的曲线,下列分析正确的是( )
如图是A、B、C三种物质的曲线,下列分析正确的是( )| A. | 50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C | |
| B. | 50℃100gA溶液中含A的质量为50g | |
| C. | 将C的饱和溶液变为不饱和溶液,采用降温结晶方法 | |
| D. | 将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C |
2.分析所给数据,下列选项正确的是( )
| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氢氧化钙 | 0.18 | 0.15 | 0.12 | 0.11 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
| A. | 将50℃的氢氧化钙饱和溶液降温会析出晶体 | |
| B. | 30℃硝酸钾的饱和溶液溶质的质量分数为45.8% | |
| C. | 50℃时不可能配得溶质质量分数相等的硝酸钾、氢氧化钙两种溶液 | |
| D. | 硝酸钾的饱和溶液升高温度后还可以继续溶解硝酸钾固体 |