题目内容
2.根据下列实验装置图,回答问题:| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室中若用装置A制取氧气,化学反应方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,若要收集一瓶较纯净的氧气,应选用的收集装置为C(填字母),若用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;
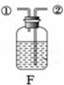
(3)实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,可选择的发生装置和收集装置的组合为BD(填字母),检验二氧化碳是否集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口(填“①”或“②”)通入.
分析 (1)熟记仪器的名称;
(2)根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,排水法收集的氧气纯净,以及收集氧气的正确操作进行分析;
(3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,该反应的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,溶于水,二氧化碳不具有助燃性,浓硫酸有吸水性,洗气应该是长进短出进行分析.
解答 解:(1)a是酒精灯,b是长颈漏斗;故填:酒精灯;长颈漏斗;
(2)A装置适用于固体加热制取氧气,且试管口没有棉花团,所以是加热氯酸钾与二氧化锰的混合物制取氧气,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,排水法收集的氧气纯净,所以要收集一瓶较纯净的氧气,应选用的收集装置为C,用该方法收集到的氧气中混有空气,可能的原因是导管口刚有气泡冒出时就收集了;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;C;导管口刚有气泡冒出时就收集了;
(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,溶于水,所以可选择的发生装置和收集装置的组合为BD,二氧化碳不具有助燃性,所以检验二氧化碳是否集满的方法是:将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,浓硫酸有吸水性,洗气应该是长进短出,所以用该方法制得的二氧化碳中常混有少量水蒸气,可用F装置除去,则F装置中应盛有的物质为浓硫酸,该混合气体应从F装置的②口通入.
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑,BD,将燃着的木条放在集气瓶口,若木条熄灭,证明已集满,浓硫酸,②.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案| A. | 不同种元素组成的物质一定是化合物 | |
| B. | 先加稀盐酸无明显现象,再加BaCl2溶液产生白色沉淀,证明溶液中一定含有SO42- | |
| C. | 使紫色石蕊试液变红色的无色气体一定是二氧化碳气体 | |
| D. | 有单质和化合物生成的反应一定是置换反应 |
| A. | 分别测密度 | B. | 用澄清石灰水区别 | ||
| C. | 用带火星的木条区别 | D. | 用燃着的木条区别 |
| A. | CH20 | B. | C2H4 | C. | CH4O | D. | CH4 |

 如图为某钙片的商品标签,根据标签的有关信息,某儿童按标签用量服药,每天补充钙元素质量是0.6g.
如图为某钙片的商品标签,根据标签的有关信息,某儿童按标签用量服药,每天补充钙元素质量是0.6g.