题目内容
19. 黄铜是由铜和锌组成的合金,当含锌量小于35%时,塑性好,适于冷热加压加工、若增
黄铜是由铜和锌组成的合金,当含锌量小于35%时,塑性好,适于冷热加压加工、若增加锌的含量、则黄铜抗拉强度逐渐下降,甚至无使用价值,某兴趣小组对某黄铜样品进行探究,称取样品10.0g,再用100.0g稀硫酸溶液逐滴滴入,实验情况如图所示,求:
(1)铜锌合金中,Zn的质量是3.25g;
(2)所用稀硫酸溶液中溶质的质量分数是多少?(请写出解题过程)
分析 根据题意,锌与稀硫酸反应生成硫酸锌和氢气;由反应的实验情况图,完全反应后剩余固体的质量为6.75g,即铜锌合金样品中含铜的质量为6.75g,则锌的质量为10g-6.75g=3.25g;由参加反应的锌的质量,计算出参加反应硫酸的质量,进而可计算出所用稀硫酸溶液中溶质的质量分数.
解答 解:(1)由反应的实验情况图,完全反应后剩余固体的质量为6.75g,即铜锌合金样品中含铜的质量为6.75g,则锌的质量为10g-6.75g=3.25g.
(2)设反应中消耗稀硫酸溶液中溶质的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 98
3.25g x
$\frac{65}{3.25g}=\frac{98}{x}$
x=4.9g
所用稀硫酸溶液中溶质的质量分数为:$\frac{4.9g}{100g}$×100%=4.9%.
答:所用稀硫酸溶液中溶质的质量分数是4.9%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图表信息,确定铜的质量为6.75g的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
9.下列化肥中属于复合肥的是( )
| A. | KNO3 | B. | 钙镁磷肥 | C. | Ca(H2PO4)2 | D. | NH4NO3 |
10.由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%.取该混合物5g,将其投入115g的稀硫酸中恰好完全反应,所得溶液中溶质的质量分数为( )
| A. | 5% | B. | 15% | C. | 10% | D. | 20% |
14.归纳总结能使知识系统化,有利于提高素质和能力.下面是一同学对部分化学知识的归纳,其中都正确的一项是( )
| A.物质的检验 | B.物质的鉴别 |
| ①氧气一带火星的木条 ②二氧化碳--澄清的石灰水 | ①稀盐酸和稀硫酸--加入石蕊试液 ②氧化铜和氧化镁一观察颜色 |
| C.物质的除杂 | D.物质的制备 |
| ①二氧化碳(一氧化碳)--点燃 ②铁(铜)--氯化铜溶液 | ①生石灰--高温煅烧熟石灰 ②氢气一银片和稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
4. 自制的简易净水器如图所示,浑浊的河水变成清水.其中细沙的作用是( )
自制的简易净水器如图所示,浑浊的河水变成清水.其中细沙的作用是( )
 自制的简易净水器如图所示,浑浊的河水变成清水.其中细沙的作用是( )
自制的简易净水器如图所示,浑浊的河水变成清水.其中细沙的作用是( )| A. | 沉淀 | B. | 吸附 | C. | 过滤 | D. | 消毒 |
8.水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )
| A. | 用过滤的方法可以使硬水软化 | |
| B. | 用活性炭吸附水中的色素和异味是化学变化 | |
| C. | 水通电分解产生氢气和氧气质量比为2:1 | |
| D. | 水发生三态变化时,发生的是物理变化 |
18.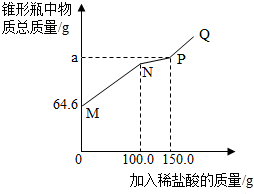 取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )
取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )
 取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )
取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )| A. | N点的溶液表示氢氧化钠被恰好完全反应 | |
| B. | PQ段(不含P点)溶液的pH<7 | |
| C. | NP段表示产生气体的过程,a的值为210.2 | |
| D. | 该固体样品中氢氧化钠的质量为8.0g |
