题目内容
将一定质量的金属锌投入到100g稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示.试求:
(1)完全反应后生成H2的质量为 g;
(2)所用硫酸溶液中溶质的质量分数.

| 根据化学反应方程式的计算;有关溶质质量分数的简单计算.菁优网版权所有 | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | 根据图中数据可以判断生成氢气的质量; 根据氢气的质量可以计算稀硫酸中硫酸的质量,进一步可以计算所用硫酸溶液中溶质的质量分数. |
| 解答: | 解:(1)由图中可知,完全反应后生成H2的质量为0.4g. 故填:0.4. (2)设所用硫酸溶液中溶质的质量为x, Zn+H2SO4═ZnSO4+H2↑, 98 2 x 0.4g
x=19.6g, 所用硫酸溶液中溶质的质量分数为: 答:所用硫酸溶液中溶质的质量分数为19.6%. |
| 点评: | 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性. |

练习册系列答案
相关题目
节能减排,保护环境,伊娃美丽广安,是我们共同的责任.下列做法中,与此倡导不相符的是( )
|
| A. | 提倡使用一次性发泡塑料餐具和塑料袋 |
|
| B. | 合理使用化肥、农药 |
|
| C. | 发展快速公交、减少私家车出行 |
|
| D. | 提倡使用无磷洗衣粉 |
下列四种物质中,属于化合物的是( )
|
| A. | 生铁 | B. | 冰水混合物 | C. | 食盐溶液 | D. | 液氧 |
合理搭配饮食是我们的健康理念,中考期间,小明妈妈为他准备了一份午餐:馒头、红烧肉、豆腐汤、炸鸡腿,你认为这份午餐搭配中还应添加下列食口中的( )
|
| A. | 黄瓜 | B. | 牛奶 | C. | 炒鸡蛋 | D. | 烤野兔肉 |
|
|
|
|
|
|
|
|
|
|
 =
= ,
, ×100%=19.6%,
×100%=19.6%,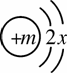 ⑵右图是某粒子的结构示意图。
⑵右图是某粒子的结构示意图。