题目内容
(1)按下列要求选择序号填空。
A. CH4 B .2Fe3+ C .CO32- D.3O3 E.OH- F .C2H5OH G .3O2 H. 2Fe2+
①两个亚铁离子_____▲_______ ; ②天然气的主要成分____▲______ ;
③纯碱中的阴离子____▲______ ; ④ 3个氧分子____ _▲________。
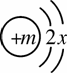 ⑵右图是某粒子的结构示意图。
⑵右图是某粒子的结构示意图。
①若该粒子为阳离子时,则m - 2__▲__ x<(选填“>”“<”或“=”);
②若该粒子为原子,且m = 3x时,则该元素属于__▲__ 元素(填“金属” 或“非金属”);
(3)钢铁制品在 中易生锈;请写出一种防止铁生锈的方法 ,由于 不同,使得钢和生铁的坚韧性有较大差异。
⑴①H ② A ③ C ④ G ⑵ ① > ② 金属 ⑶潮湿的空气中;涂油等(答案合理同样给分);含碳量不同

下列化学方程式书写正确的是
A.硫在空气中燃烧: S+ O2  SO2
SO2
B.铁与稀硫酸反应: 2 Fe + 3H2SO4=== F e2(SO4)3 +3 H2
e2(SO4)3 +3 H2
 |
C. 乙
乙 醇在空气中燃烧: C2H5OH + 3O2 2CO2↑ + 3H2O
醇在空气中燃烧: C2H5OH + 3O2 2CO2↑ + 3H2O
D.木炭与氧化铜在高温下反应:CuO + C  Cu + CO2↑
Cu + CO2↑
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
①制备氧化铜并检验产物,装置如下图所示(省略夹持仪器):
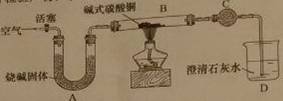
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |



| |
 请在中填入配平后的系数(10)。
请在中填入配平后的系数(10)。
C中试剂是(11)。A的作用是吸收空气中的(12),防止对产物检验造成干扰。选择t3时停止加热的理由是(13)。
② 一定量碳粉还原①中制得的氧化铜并检验产物,装置如下图所示:
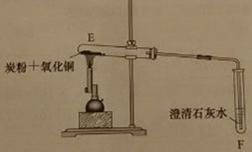
实验过程中,观察到F中溶液变浑浊,E中的现象是(14)。
反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是(15)。
③ 分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因。
(16)