题目内容
用废铜屑制取硫酸铜,有甲、乙两种实验方案可供选择:
甲方案:铜屑
硫酸铜
[Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O]
乙方案:铜屑
氧化铜
硫酸铜
(1)请写出乙方案中有关反应的化学方程式.
(2)你认为甲、乙两种方案哪个更合理?简要说明理由.
甲方案:铜屑
| 浓硫酸 |
| △ |
[Cu+2H2SO4(浓)
| ||
乙方案:铜屑
| 空气中 |
| △ |
| 硫酸 |
(1)请写出乙方案中有关反应的化学方程式.
(2)你认为甲、乙两种方案哪个更合理?简要说明理由.
考点:化学实验方案设计与评价,书写化学方程式、文字表达式、电离方程式
专题:简单实验方案的设计与评价
分析:(1)据书写化学方程式的原则和方法进行书写;
(2)对于实验装置的评价,还要考虑实验优劣对比,要注意从科学性、可行性,还有对环境等的影响等来考虑.在分析时要注意对实验装置和装置下的原理的细节的分析对比,从中提取答案
(2)对于实验装置的评价,还要考虑实验优劣对比,要注意从科学性、可行性,还有对环境等的影响等来考虑.在分析时要注意对实验装置和装置下的原理的细节的分析对比,从中提取答案
解答:解:(1)铜与空气中的氧气在加热的条件下会生成黑色的氧化铜:2CuO+O2
2CuO;氧化铜与硫酸反应生成硫酸铜和水:CuO+H2SO4═CuSO4+2H2O.
(2)当制取相同质量的硫酸铜时,甲方案消耗掉的硫酸多一倍,且多余出来的硫酸对应的产物为有毒的二氧化硫.
故答案为:(1)2CuO+O2
2CuO;CuO+H2SO4═CuSO4+2H2O;
(2)乙方案;此方案既可节省原料又可避免产生SO2污染空气.
| ||
(2)当制取相同质量的硫酸铜时,甲方案消耗掉的硫酸多一倍,且多余出来的硫酸对应的产物为有毒的二氧化硫.
故答案为:(1)2CuO+O2
| ||
(2)乙方案;此方案既可节省原料又可避免产生SO2污染空气.
点评:实验设计的评价要注意从实验本身去分析,要注意从科学性、可行性的方面进行分析归纳.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列关于醋酸(C2H4O2)的说法中,不正确的是( )
| A、由三种元素组成 |
| B、由8个原子构成 |
| C、氧元素的质量分数最大 |
| D、碳、氢、氧原子的个数比为1:2:1 |


 实验室利用如图所示装置进行蒸发的实验.
实验室利用如图所示装置进行蒸发的实验. 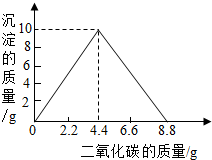 某实验小组在一定量的石灰水中通入CO2,产生沉淀的质量与通入CO2质量的关系如图所示.已知反应CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2易溶于水.
某实验小组在一定量的石灰水中通入CO2,产生沉淀的质量与通入CO2质量的关系如图所示.已知反应CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2易溶于水. 如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的气体.常温下,丁为黑色固体,戊为紫红色金属;G是一种具有刺激性气味的气体,其水溶液呈碱性,工业上用甲和丙化合制备G;农业上常用F改良酸性土壤(如图中部分反应条件已省略).回答下列问题:
如图中的物质均为初中化学常见的物质.其中甲、乙、丙、丁、戊均为单质,丙是空气中含量最多的气体.常温下,丁为黑色固体,戊为紫红色金属;G是一种具有刺激性气味的气体,其水溶液呈碱性,工业上用甲和丙化合制备G;农业上常用F改良酸性土壤(如图中部分反应条件已省略).回答下列问题: (1)如图为垃圾箱上的标志.
(1)如图为垃圾箱上的标志.