题目内容
(1)完成下列反应的化学方程式
①BaCl2+Na2SO4=
②Ba(OH)2+2HNO3=
(2)上述反应之所以能够发生,是因为这些反应物中有一些“特殊”的阴、阳离子,它们能相互结合,如上述反应①中,实际参加反应的离子是Ba2+和SO42-,而Cl-、Na+则是旁观者,并没有参加反应.请你分析上述反应②中实际参加反应的离子是 .
(3)请根据你的想象,在如图右边的容器中画出体现NaOH和稀HCl反应产物的示意图.

①BaCl2+Na2SO4=
②Ba(OH)2+2HNO3=
(2)上述反应之所以能够发生,是因为这些反应物中有一些“特殊”的阴、阳离子,它们能相互结合,如上述反应①中,实际参加反应的离子是Ba2+和SO42-,而Cl-、Na+则是旁观者,并没有参加反应.请你分析上述反应②中实际参加反应的离子是
(3)请根据你的想象,在如图右边的容器中画出体现NaOH和稀HCl反应产物的示意图.

考点:复分解反应的条件与实质,中和反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学反应的基本类型和能量变化
分析:根据已有的知识进行分析解答,氯化钡能与硫酸钠反应生成硫酸钡沉淀和氯化钠,氢氧化钡能与硝酸反应生成硝酸钡和水;复分解反应的实质是酸碱盐中的离子互相交换成分生成了水、气体或沉淀,据此解答.
解答:解:
(1)①氯化钡能与硫酸钠反应生成硫酸钡沉淀和氯化钠,故答案为:BaCl2+Na2SO4=BaSO4↓+2NaCl.
②氢氧化钡能与硝酸反应生成硝酸钡和水,故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O.
(2)根据信息可知能结合成水或气体或沉淀的,即为实际参加的离子,②②中实际参加反应的离子是H+和OH-,故答案为:H+和OH-;
(3)因反应生成水,则H+、OH-实际参加反应,Cl-、Na+则实际不参加反应,即反应前后不变,故答案为:
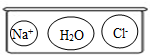
(1)①氯化钡能与硫酸钠反应生成硫酸钡沉淀和氯化钠,故答案为:BaCl2+Na2SO4=BaSO4↓+2NaCl.
②氢氧化钡能与硝酸反应生成硝酸钡和水,故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O.
(2)根据信息可知能结合成水或气体或沉淀的,即为实际参加的离子,②②中实际参加反应的离子是H+和OH-,故答案为:H+和OH-;
(3)因反应生成水,则H+、OH-实际参加反应,Cl-、Na+则实际不参加反应,即反应前后不变,故答案为:

点评:本题考查了复分解反应的实质,完成此题,可以依据复分解反应的条件进行.

练习册系列答案
相关题目
金属X、Y、Z分别是铁、铝、铜、银中的一种,其中X能与稀硫酸反应生成X2(SO4)3,而Y、Z不能与稀硫酸反应,Y能与硝酸银溶液反应,而Z不能与硝酸银溶液反应.则X、Y、Z依次为( )
| A、铁、银、铜 |
| B、铁、铜、银 |
| C、铝、铜、银 |
| D、铝、银、铜 |



