题目内容
3.如图是用一氧化碳还原氧化铜的实验装置图.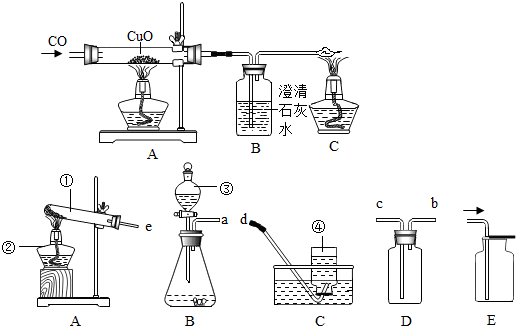
(1)先通入一氧化碳,过一会儿再给氧化铜加热的原因是排除玻璃管内的空气,防止加热时发生爆炸.
(2)根据实验事实填写如表:
| 观察到的现象 | 所发生现象的化学方程式 | |
| A处(CuO处) | 黑色固体逐渐变成红色固体 | CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2 |
| B处(澄清石灰水中) | 澄清石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H2O |
| C处 | 尾气燃烧发生蓝色火焰 | 2C0+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
(4)、写出编号①②③④的仪器名称:
①试管; ②酒精灯;
③分液漏斗; ④集气瓶.
分析 (1)根据一氧化碳的可燃性分析解答;
(2)根据一氧化碳还原氧化铜的产物分析反应的现象;
(3)根据一氧化碳的毒性及可燃性进行分析;
(4)根据实验室常用仪器的名称和题中所指仪器的作用进行分析.
解答 解:(1)一氧化碳具有可燃性,点燃一氧化碳与空气的混合气体时可能发生爆炸,因此实验开始时要先通一会一氧化碳,排除玻璃管内的空气,防止加热时发生爆炸;
(2)一氧化碳与氧化铜在高温的条件下生成铜和二氧化碳,黑色粉末变成红色,生成的二氧化碳使澄清石灰水变浑浊,尾气中一氧化碳燃烧发出蓝色火焰;
(3)一氧化碳有毒,不能直接排放到空气中,因此C处放置点燃的酒精灯的目的是燃烧尾气中的CO,防止污染空气;
(4)通过分析题中所指仪器的作用可知,①是试管,②是酒精灯,③是分液漏斗,④是集气瓶.
故答案为(1)排除玻璃管内的空气,防止加热时发生爆炸;
| 黑色固体逐渐变成红色固体 | CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2 |
| 澄清石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H20 |
| 尾气燃烧发生蓝色火焰 | 2C0+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
(4)试管,酒精灯,分液漏斗,集气瓶.
点评 一氧化碳还原氧化铜实验步骤:实验开始先通一氧化碳,排净空气再点燃酒精灯,黑色变红之后先撤酒精灯,继续通一氧化碳直到玻璃管冷却.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
11.下列说法正确的是( )
| A. | 将25gKCl溶液蒸干得到5gKCl固体,则原溶液中溶质的质量分数为20% | |
| B. | 某物质中只含有一种元素,则该物质一定是纯净物 | |
| C. | 只有一种元素的阳离子和一种元素的阴离子构成的物质一定是纯净物 | |
| D. | 盐形成的溶液中,既不能电离出H+,也不能电离出OH- |
15.某同学摘花时,被蜜蜂蜇伤.蜜蜂的刺液是酸性的,以下家庭常见物品可以用来涂抹在蜇伤处以减轻疼痛的是( )
| A. | 食醋(pH约为3) | B. | 牛奶(pH约为6.5) | C. | 矿泉水(pH约为7) | D. | 肥皂水(pH约为10) |
 去年,我国部分地区爆发了H7N9禽流感.为了防止禽流感蔓延,人们将家禽捕杀、掩埋,并在禽舍和掩埋坑中洒上大量热石灰.
去年,我国部分地区爆发了H7N9禽流感.为了防止禽流感蔓延,人们将家禽捕杀、掩埋,并在禽舍和掩埋坑中洒上大量热石灰.