题目内容
18.用化学符号填空:(1)①盐酸、硫酸都能使紫色石蕊溶液变红的原因是溶液中都存在H+;
②高锰酸钾中锰元素的化合价K$\stackrel{+7}{Mn}$O4.
(2)①盐酸除铁锈的反应方程式Fe2O3+6HCl═2FeCl3+3H2O;
②只选用一种溶液和金属丝、通过一次反应就能将铁、铜、银的活动性验证出来,发生反应的方程式是Fe+CuSO4=Cu+FeSO4(可放性答案,合理即可).
分析 (1)①盐酸、硫酸都能使紫色石蕊溶液变红的原因是溶液中都存在氢离子.
②化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)①盐酸、硫酸都能使紫色石蕊溶液变红的原因是溶液中都存在氢离子,其离子符号为:H+.
②高锰酸钾中钾元素显+1价,氧元素显-2价,锰元素显+7价;由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故高锰酸钾中锰元素的化合价可表示为:K$\stackrel{+7}{Mn}$O4.
(2)①铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.
②只选用一种溶液和金属丝、通过一次反应就能将铁、铜、银的活动性验证出来,可采用将铁、银分别放入硫酸铜溶液中,铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,银不硝酸铜溶液反应,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4(可放性答案,合理即可).
故答案为:(1)①H+;②K$\stackrel{+7}{Mn}$O4;(2)①Fe2O3+6HCl═2FeCl3+3H2O;②Fe+CuSO4=Cu+FeSO4(可放性答案,合理即可).
点评 本题难度不大,掌握常见化学用语(化学方程式、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
相关题目
6.已知亚硫酸钠对应的亚硫酸盐中硫元素的化合价为+4,则亚硫酸钠的化学式为( )
| A. | H2SO4 | B. | SO2 | C. | Na2SO3 | D. | H2SO3 |
3.如图是用一氧化碳还原氧化铜的实验装置图.
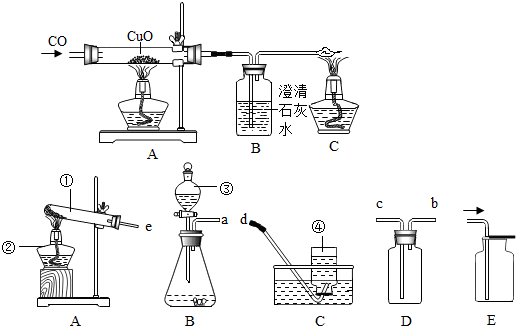
(1)先通入一氧化碳,过一会儿再给氧化铜加热的原因是排除玻璃管内的空气,防止加热时发生爆炸.
(2)根据实验事实填写如表:
(3)C处为什么要放一个点燃的酒精灯?
(4)、写出编号①②③④的仪器名称:
①试管; ②酒精灯;
③分液漏斗; ④集气瓶.

(1)先通入一氧化碳,过一会儿再给氧化铜加热的原因是排除玻璃管内的空气,防止加热时发生爆炸.
(2)根据实验事实填写如表:
| 观察到的现象 | 所发生现象的化学方程式 | |
| A处(CuO处) | 黑色固体逐渐变成红色固体 | CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2 |
| B处(澄清石灰水中) | 澄清石灰水变浑浊 | Ca(OH)2+CO2═CaCO3↓+H2O |
| C处 | 尾气燃烧发生蓝色火焰 | 2C0+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
(4)、写出编号①②③④的仪器名称:
①试管; ②酒精灯;
③分液漏斗; ④集气瓶.
2.分离、除杂和检验是化学实验的重要环节,下列实验设计能达到目的是
( )
| 实验内容 | 实验设计 | |
| A | 除去铜粉中少量的铁粉 | 加入足量的稀硫酸,过滤,蒸发 |
| B | 提纯含有少量NaCl的KNO3固体 | 先加入水溶解,蒸发结晶 |
| C | 区分NH4HCO3和NH4Cl | 取样,加稀盐酸,观察是否有气泡产生 |
| D | 分离CO2和CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向剩余溶液中加浓盐酸,即可“释放”出纯净的CO2 |
| A. | A | B. | B | C. | C | D. | D |
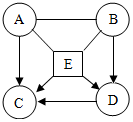 已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应
已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应 如图中A~J均为初中化学中的常见物质,其中仅C、H、I为单质.A为大理石的主要成分.J由两种元素组成,且其溶液为浅绿色.(反应条件均已省略)
如图中A~J均为初中化学中的常见物质,其中仅C、H、I为单质.A为大理石的主要成分.J由两种元素组成,且其溶液为浅绿色.(反应条件均已省略)