题目内容
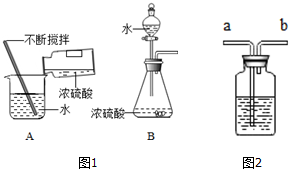
7. “嫦娥一号”飞船的成功发射是我国航天事业的又一里程碑.金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;(过氧化钠还能与盐酸、水等物质发生反应产生氧气)为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图1所示的实验.
“嫦娥一号”飞船的成功发射是我国航天事业的又一里程碑.金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;(过氧化钠还能与盐酸、水等物质发生反应产生氧气)为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图1所示的实验.(1)制取CO2的装置,应从下列图2、图3、图4中选择图3.
(2)检查图3装置的气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到漏斗颈中形成一段稳定的水柱现象,即可证明装置不漏气.
(3)设计A、B装置的目的是净化导入的纯净且干燥的CO2.其中,①A装置的具体功能是吸收二氧化碳中混有的氯化氢气体所发生的化学方程式是NaHCO3+HCl═NaCl+H2O+CO2↑;②B装置的具体功能是干燥二氧化碳,其瓶内液体应是浓硫酸;
(4)为了确定CO2跟Na2O2反应产生的气体是氧气,最后还要采用的验证实验操作是将带火星的木条放在集气瓶上方的导管口附近.
(5)表明二氧化碳没有被过氧化钠完全吸收的现象是C装置处的澄清石灰水变浑浊.
分析 (1)根据发生装置的选择关键看反应物的状态,是否需要加热,制取二氧化碳不需要加热,所以图1不对,图3中长颈漏斗末端在液面以上,气体容易逸出,也不对进行分析;
(2)根据只要是不漏气,在一个封闭体系中,长颈漏斗内液面不会发生变化进行分析;
(3)设计A、B装置的目的是净化导入的纯净且干燥的CO2,即除去二氧化碳中的杂质,因为制取二氧化碳需要盐酸,所以二氧化碳中会混有水蒸气和氯化氢气体,A装置是除氯化氢气体的,B装置是除水蒸气的;
(4)验证氧气的方法是使用带火星的木条;
(5)验证二氧化碳的存在就是利用澄清石灰水.
解答 解:(1)发生装置的选择,要考虑反应物的状态和反应条件,固体与固体制气体需要加热,固体与液体制气体不需要加热;
实验室制取二氧化碳不需要加热,并且长颈漏斗末端必须在液面以下,否则气体会逸出,所以选择:图3;
(2)如果装置漏气的话,由于连通器的原理,长颈漏斗内外液面会相平,不漏气,长颈漏斗内液面不再下降;
(3)因为实验室制二氧化碳用的是盐酸,所以制取的二氧化碳中会混有水蒸气和氯化氢气体,图A是除去氯化氢气体的装置,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
图B是除去水蒸气的,如果顺序颠倒,水蒸气就白除了,又会混上水蒸气;
(4)验证氧气的方法是使用带火星的木条,能够使带火星的木条复燃,说明是氧气;
(5)表明二氧化碳没有被过氧化钠完全吸收,也就是说还存在二氧化碳,将气体通过澄清石灰水,变浑浊说明二氧化碳没有被过氧化钠完全吸收.
故答案为:(1)图3;
(2)漏斗颈中形成一段稳定的水柱;
(3)①吸收二氧化碳中混有的氯化氢气体,NaHCO3+HCl═NaCl+H2O+CO2↑;
②干燥二氧化碳,浓硫酸;
(4)将带火星的木条放在集气瓶上方的导管口附近;
(5)C装置处的澄清石灰水变浑浊.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 矿泉水 | B. | 二氧化碳 | C. | 食盐水 | D. | 铁 |

(1)步骤1所需玻璃仪器是烧杯、玻璃棒;步骤3的操作名称是过滤.
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠
假设2:只含有氢氧化钠
假设3:氯化钠和氢氧化钠都含有
(3)设计实验方案,进行试验.
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液.回答下列问题:
①加入过量试剂A的名称是硝酸钡溶液.加入试剂A 的目的是d;(填字母编号)
a.检验OH-离子 b.检验Cl-离子
c.除去CO32-离子 d.避免对Cl-或OH-的检验的干扰
②填写下表:
| 实验步骤 | 预期现象和结论 |
| 步骤4:取少量滤液于试管,往其中滴加2~3滴酚酞试液 | ①如果酚酞变红,假设2或3成立. ②如果酚酞不变红,假设1成立. |
| 步骤5:向上步中使酚酞变成红色的试管中滴加足量的稀硝酸至溶液呈酸性,再滴加硝酸银溶液. | ①若没有白色沉淀生成,则说明假设1或3成立. ②若有白色沉淀生成,则说明2成立. |
| A. | 只有①②③ | B. | 只有②③④ | C. | 只有①②③④ | D. | 全部都是 |
| 农作物 | 水稻 | 茶树 | 玉米 | 马铃薯 |
| pH | 6.0~7.0 | 6.9~7.0 | 7.8~8.1 | 4.8~5.5 |
| A. | 玉米 | B. | 茶数 | C. | 水稻 | D. | 马铃薯 |
 如图所示它演示在什么条件下容易生锈,实验中看到的现象是B处的铁生锈最快最多,原因是该处既可与水接触又可与氧气接触.根据该实验验证铁生锈条件可以推知铁锈中一定含有的元素是铁、氢、氧.
如图所示它演示在什么条件下容易生锈,实验中看到的现象是B处的铁生锈最快最多,原因是该处既可与水接触又可与氧气接触.根据该实验验证铁生锈条件可以推知铁锈中一定含有的元素是铁、氢、氧.