题目内容
10.将硫酸氢钠溶液滴入盛有锌粒的试管中,可以观察到锌粒表面有气泡产生,该反应的化学方程式为:Zn+2NaHSO4=ZnSO4+Na2SO4+H2↑,某同学就该实验的现象及反应化学方程式,得出以下结论,其中正确的是( )| A. | 单质跟化合物反应生成新的单质和新的化合物的反应一定是置换反应 | |
| B. | 上述反应中,金属锌变成锌离子进入溶液,实际上是金属得到了电子 | |
| C. | 硫酸氢钠电离时产生的阳离子含氢离子,故硫酸氢钠溶液呈酸性 | |
| D. | 硫酸氢钠与金属锌反应后的产物是盐和氢气,符合酸的共性,硫酸氢钠属于酸类 |
分析 A、根据置换反应的定义考虑;
B、根据锌由原子变为离子的方法考虑;
C、根据酸性溶液的特征分析.
D、根据酸的定义考虑,电离时,电离出来的阳离子全部是氢离子的化合物属于酸.
解答 解:A、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,该反应的生成物中含有两种化合物,所以不属于置换反应,故A错;
B、锌由原子变为离子失去两个电子,故B错误;
C、硫酸氢钠电离时产生的阳离子中含有氢离子,因此溶液呈酸性,故C正确;
D、电离时,电离出来的阳离子全部是氢离子的化合物属于酸,硫酸氢钠电离出来的阳离子中不仅含有氢离子,还含有钠离子,不属于酸,属于盐,故D错误;
故选:C.
点评 本题属于信息题的考查,解答本题关键是要知道置换反应的定义,熟悉酸、碱、盐的定义和判断方法.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目
1.下列实验基本操作正确的是( )
| A. | 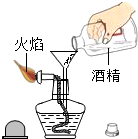 | B. | 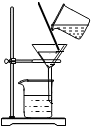 | C. | 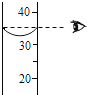 | D. | 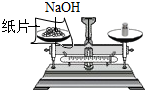 |
5.A、B、C三种固体物质的溶解度曲线如图所示.有关叙述正确的是( )


| A. | t1℃时,A、B、C的溶解度大小关系是A>B=C | |
| B. | t2℃时,将A、B、C各25 g分别放入100g水中,能形成饱和溶液的物质是A、B | |
| C. | A中混有少量B,可通过降温结晶提纯A | |
| D. | 将A、B、C各饱和溶液从t2℃时降至t1℃时,析出晶体最多的是A |
15.物质是由肉眼看不到的分子、原子和离子等微观粒子构成的.如图是甲烷气体发生反应的微观示意图,下列说法错误的是( )
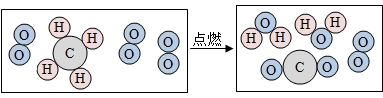

| A. | 该反应中甲烷分子和水分子的个数比是1:2 | |
| B. | 该反应的生成物有3种物质 | |
| C. | 该反应发生的条件是点燃,化学反应前后原子的种类和数目不变 | |
| D. | 该模型可说明:化学变化的实质是分子分成原子,原子重新组合成新分子 |
2.科学实验要规范操作,下列初中科学实验操作你认为不正确的是( )
| A. |  二氧化碳的验满 | B. |  倾倒液体 倾倒液体 | C. |  检验气密性 检验气密性 | D. |  加热液体 |
19.下列实验操作中,正确的是( )
| A. |  取用固体药品 | B. |  闻药品味道 | ||
| C. |  用100mL量筒量取8.5mL盐酸 | D. |  滴加液体 |
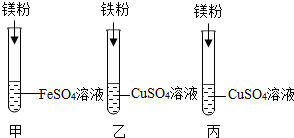 某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:
某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:
