题目内容
17.工业上用煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳.现用15kg石灰石制取二氧化碳4.4kg,则石灰石中碳酸钙的质量是多少?石灰石中碳酸钙的质量分数是多少?分析 根据要制取二氧化碳的质量,由反应的化学方程式计算出碳酸钙的质量分数即可解答.
解答 解:设石灰石中碳酸钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 4.4kg
$\frac{100}{x}=\frac{44}{4.4kg}$
x=10kg
石灰石中碳酸钙的质量分数是:$\frac{10kg}{15kg}×100%$=66.7%.
答:石灰石中碳酸钙的质量是10kg,石灰石中碳酸钙的质量分数为66.7%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
8.对下列事实的解释错误的是( )
| 事实 | 解释 | |
| A | 打开盛有浓盐酸的瓶盖,瓶口出现白雾 | 浓盐酸有挥发性 |
| B | 浓硫酸敞口放置在空气中变稀 | 浓硫酸具有吸水性 |
| C | 将活性炭放入冰箱中,可出去异味 | 活性炭具有吸附性 |
| D | 烧碱放在烧杯中变质 | 烧碱易潮解 |
| A. | A | B. | B | C. | C | D. | D |
5.下列实验操作正确的是( )
| A. | 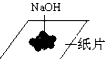 称量固体 | B. | 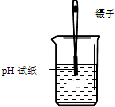 测定溶液pH | C. | 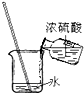 稀释浓硫酸 | D. |  滴加液体 |
2.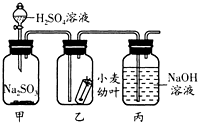 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.
(1)写出产生二氧化硫的化学方程式Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)在实验中,丙装置的作用是吸收未反应的二氧化硫,防止污染空气;
(3)其他实验条件相同情况下,该小组观察到小麦幼叶在不同光照强度下,叶片发生变化时间不同,如下表所示.结合叶的结构知识,请你解释为何光照的强弱会影响二氧化硫对植物的危害?光照的强弱会影响叶表皮气孔的开放程度,进而导致二氧化硫对植物的危害随光照的加强而增大.
 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.(1)写出产生二氧化硫的化学方程式Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)在实验中,丙装置的作用是吸收未反应的二氧化硫,防止污染空气;
(3)其他实验条件相同情况下,该小组观察到小麦幼叶在不同光照强度下,叶片发生变化时间不同,如下表所示.结合叶的结构知识,请你解释为何光照的强弱会影响二氧化硫对植物的危害?光照的强弱会影响叶表皮气孔的开放程度,进而导致二氧化硫对植物的危害随光照的加强而增大.
| 室内 | 阳光下 | ||
| 出现烟斑时间 | 叶片变黄时间 | 出现烟斑时间 | 叶片变黄时间 |
| 30分钟 | 38分钟 | 15分钟 | 23分钟 |
7.下列实验操作中,先后顺序不正确的是( )
| A. | 加热前,试管外壁有水,应该先擦干再加热 | |
| B. | 实验室用高锰酸钾加热制取氧气时,反应完毕后,应先撤去酒精灯,再从水槽中取出导气管 | |
| C. | 实验室制取氧气时,应先检查装置的气密性,再加入药品 | |
| D. | 对试管中的物体加热时,应先来回均匀受热再定点加热 |
