题目内容
图中字母A~I分别表示不同的常见物质.“→”表示物质间存在转化关系,部分反应条件和部分生成物已略去.请回答下列问题:?

(1)反应①的基本反应类型为 .?
(2)写出与C具有相同元素组成的另一种物质的名称 .?
(3)写出G的化学式 .?
(4)写出反应②的化学方程式 .
解答:解:B是红棕色固体,则B是氧化铁,能与单质C反应生成单质E和F,则C是碳,E是铁,F是二氧化碳,二氧化碳能与碳高温反应生成气体G,则G是一氧化碳,一氧化碳能与B加热反应生成紫红色单质H,则H是铜,B是氧化铜,铁能与D反应生成浅绿色溶液I和铜,则是铁与铜盐溶液的置换反应,D由黑色固体A与盐酸反应生成,则D是氯化铜,A是氧化铜,代入框图,推断合理;
(1)反应①是氧化铁与碳高温反应生成铁和二氧化碳,此反应是一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,属于置换反应,故填:置换反应;
(2)C是碳,与其具有相同元素的物质可以是石墨,故填:石墨;
(3)G是一氧化碳,故填:CO;
(4)E是铁,D是氯化铜,铁能与氯化铜反应生成氯化亚铁和铜,故填:Fe+CuCl2=FeCl2+Cu.
点评:本题为框图式物质推断题,完成此题,可以依据物质的性质进行,要求同学们熟练掌握常见物质的性质,以便灵活应用.

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案(24分)下图所示为实验室常用的实验装置:

(1)写出下列仪器名称:a ;b 。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置是 (填装置的字母代号),化学方程式是 ,用双氧水制取氧气的化学方程式为 。
(3)实验室用锌和稀硫酸反应制取氢气的化学方程式是 ,若将E装置中收集的氢气排出,应从 (填c或d)口通入蒸馏水。
(4)装置C相对于装置B在操作方面的优势为 。
A.可以随时加液 B.可以控制反应速率 C.可以控制反应发生与停止
同学们对美术组的环保石头纸(主要成分为碳酸钙,加入适量聚乙烯和少量胶合剂)展开探究:
[拓展实验一] 探究影响石头纸与盐酸反应快慢的因素
(5)甲、乙两同学设计实验如下:
|
|
甲 |
乙 |
|
实验过程 |
|
|
|
现象 |
试管①、②、③中产生气泡快慢的顺序为: ①>②>③。 |
|
|
分析结论 |
Ⅰ 碳酸钙与稀盐酸反应的化学方程式为 Ⅱ 对比甲同学实验①②可知, ,化学反应的速度越快; Ⅲ 对比甲同学实验 (填实验序号)可知,反应物的接触面积越大,反应速率越。 Ⅳ 乙同学的实验中,数据记录纸上应该连续记录的实验数据是 和 。 |
[拓展实验二] 测定石头纸中碳酸钙的质量分数
(6)甲组同学的方法是:(同温同压下,不同气体混合后体积等于混合前各气体体积之和。)
将样品与稀盐酸反应,测定反应后生成CO2的体积,再换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量。下图(Ⅰ)为石头纸与稀盐酸反应的装置,图(Ⅱ)用于测量CO2的体积。

① 连接仪器,夹紧弹簧夹,向a中加入一定量的水,如果a、b中有稳定的高度差,说明:装置(I)气密性 (选填“良好”或“漏气”)
② 图(Ⅱ)装置中油层的作用是_ ;
③ 反应停止后, (填序号)可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为生成二氧化碳的体积。
A. 水平移动量气管 B.上下移动量气管 C. 封闭量气管
(7) 乙组同学的实验方法是:均匀称取四份样品分别和稀盐酸反应,用电子天平及有关装置,得出二氧化碳质量,实验数据记录如下表。(其他物质既不溶于水也不跟酸反应)
|
|
第一份 |
第二份 |
第三份 |
第四份 |
|
取样品质量(g) |
6.25 |
6.25 |
6.25 |
6.25 |
|
取稀盐酸的体积(mL) |
10.0 |
20.0 |
30.0 |
40.0 |
|
产生气体的质量(g) |
0.88 |
1.76 |
2.20 |
m |
通过对数据的分析和比较,回答下列有关问题:
① 在第1份样品的实验中, 完全反应了。
② m为
③ 石头纸样品中碳酸钙的质量分数是多少?(请写出计算过程,4分)
④ 请在坐标图中画出在6.25 g样品中加入稀盐酸的体积与产生气体质量的关系图。 
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.小平和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题.
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
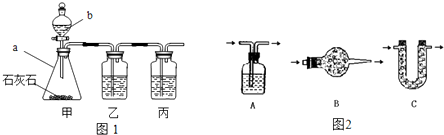
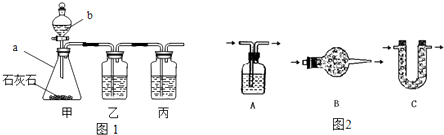
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
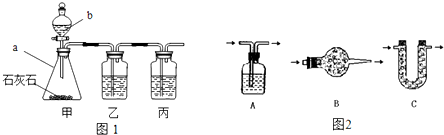
[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是________,仪器b的名称是________.装置甲中主要反应的化学方程式为________.
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去________.装置丙中主要反应的化学方程式为________.装置乙中盛有的物质是________溶液.现象:________.
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品________(选择序号);若选用B装置,则B装置中放入药品________(选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
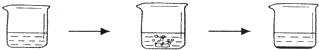
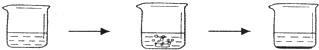
| 实验步骤 | I将适量盐酸加入烧杯中并称量 | II称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:

[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是 ,仪器b的名称是 .装置甲中主要反应的化学方程式为 .
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去 .装置丙中主要反应的化学方程式为 .装置乙中盛有的物质是 溶液.现象: .
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品 (选择序号);若选用B装置,则B装置中放入药品 (选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
| 实验步骤 | I将适量盐酸加入烧杯中并称量 | II称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III待反应完全后,称重 |
| 实验图示 | 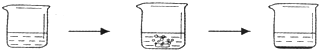 | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样的质量为12.0g | 烧杯和其中混合物的质量为107.6g |