题目内容
5.在宏观、微观和符号之间建立联系是化学学习的特点.
(1)在水、铜和氯化钠三种物质中,由分子构成的是水.
(2)在一密闭容器中,某反应前后的分子种类示意图如图所示:
①生成物中碳元素和氢元素的质量比为4:1;
②该反应的化学方程式是C2H2+H2O$\frac{\underline{\;一定条件\;}}{\;}$C2H5OH.
分析 (1)根据构成物质的微粒分析;
(2)根据微粒的构成,写出化学式、方程式,据其意义分析判断回答.
解答 解:(1)水是由水分子构成的;铜属于金属单质,是由铜原子直接构成的;氯化钠是由钠离子和氯离子构成的.
(2)①由微粒的构成可知,生成物的化学式是C2H5OH,碳元素和氢元素的质量比为:(12×2):(1×6)=4:1;
②由示意图可知,该反应是乙炔和水在一定条件下反应生成乙醇,反应的化学方程式是:C2H2+H2O$\frac{\underline{\;一定条件\;}}{\;}$C2H5OH.
故答案为:(1)水;(2)①4:1;②C2H2+H2O$\frac{\underline{\;一定条件\;}}{\;}$C2H5OH.
点评 本题难度不大,掌握物质的微观构成、化学方程式的书写是正确解答此类题的关键所在.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
13.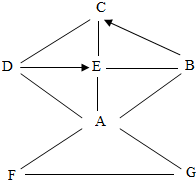 已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
 已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )
已知A、B、C、D、E、F、G均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“一”表示相互之间能反应(部分反应物、生成物以及反应条件省略).其中,A是人体胃酸的主要成分;B为一种盐;C是一种常用来灭火的气体,过多排放会导致温室效应;D是一种常用的食品干燥剂也可用做建筑材料;组成G单质的元素在地壳中含量居所有金属元素的第二位.分析以上信息及图所示,以下分析错误的是( )| A. | 物质B是可溶性的碳酸盐 | |
| B. | 物质F不可能是可溶性铜盐 | |
| C. | 物质C和D之间说明CO2和CaO在一定条件下能直接反应 | |
| D. | 以上所有物质间的转化可涉及到四个基本反应类型 |
20. 如图是甲、乙两种固体物质的溶解度曲线,下列说法中不正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,下列说法中不正确的是( )
 如图是甲、乙两种固体物质的溶解度曲线,下列说法中不正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,下列说法中不正确的是( )| A. | 20℃时,甲、乙两者的溶解度相等 | |
| B. | 大于20℃时,甲的溶解度大于乙的溶解度 | |
| C. | 40℃时,甲的饱和溶液中溶质的质量分数为33.3% | |
| D. | 将40℃乙的饱和溶液降温至20℃,可变成不饱和溶液 |
14.2015年世界水日的主题是“水与可持续发展”.下列说法正确的是( )
| A. | 冰水共存物属于纯净物 | |
| B. | 硬水和软水可用石蕊溶液来区分 | |
| C. | 有水生成的反应一定是酸和碱的中和反应 | |
| D. | 水电解时所生成氢气和氧气的质量比为2:1 |
15.通过晾晒海水或煮井盐水、盐湖水等,可以蒸发除去水分,得到粗盐,粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等).通过如图所示过程,使粗盐得到初步提纯:

(1)操作a的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)通过蒸发M溶液中的水分使之浓缩结晶,想一想,能否采用降低溶液温度的方法来达到同一目的?否(填“能”或“否”).理由是氯化钠的溶解度受温度影响变化较小.
(3)在蒸发操作时,当蒸发皿中出现较多量固体时,应停止加热,利用蒸发皿的余热使滤液蒸干.
(4)某同学欲通过实验探究所得精盐是否是纯净物,进行了如下实验.

(1)操作a的名称是过滤,该操作中要用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)通过蒸发M溶液中的水分使之浓缩结晶,想一想,能否采用降低溶液温度的方法来达到同一目的?否(填“能”或“否”).理由是氯化钠的溶解度受温度影响变化较小.
(3)在蒸发操作时,当蒸发皿中出现较多量固体时,应停止加热,利用蒸发皿的余热使滤液蒸干.
(4)某同学欲通过实验探究所得精盐是否是纯净物,进行了如下实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取一定量精盐样品于试管中,加水使之完全溶解,并向其中加入 ①碳酸钠 | ②生成白色沉淀 | 写出一个相应的化学方程式:③CaCl2+Na2CO3=CaCO3↓+2NaCl 结论:该精盐样品为混合物 |