题目内容
1.页岩气是从页岩层中开采出来的天然气,被誉为未来能源的“明星”.(1)页岩气与天然气的主要成分为甲烷.页岩气中主要成分完全燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)目前人类大量使用的三大化石能源是:石油、煤 和天然气,都属于不可再生(填“可再生”或“不可再生”)能源.为缓解能源危机,列举出需开发利用一种新能源为太阳能.
分析 (1)页岩气主要成分是甲烷,写出其燃烧的化学方程式即可;
(2)根据煤、石油和天然气属于化石燃料,是不可再生能源以及正在开发使用的新能源来解答.
解答 解:(1)页岩气主要成分是甲烷,甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;故填:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O;
(2)目前人类大量使用的三大化石能源是:石油、煤和天然气,都属于不可再生能源.为缓解能源危机,人们正积极开发利用新能源主要有太阳能、风能、氢能等;故填:煤;不可再生;太阳能.
点评 化石燃料日趋枯竭,开发利用新能源具有重要意义,人类正在开发利用的新能源有太阳能、核能、风能、水能、地热能、潮汐能、氢能等.

练习册系列答案
相关题目
9.新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化流程如图所示:
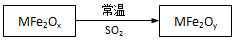
已知MFe2Oy中Fe为+3价.下列说法中,正确的是( )

已知MFe2Oy中Fe为+3价.下列说法中,正确的是( )
| A. | y的数值为5 | B. | SO2不是该反应的催化剂 | ||
| C. | MFe2Ox发生了分解反应 | D. | 该过程是物理变化 |
6.水是生命之源,也是重要的溶剂.下列有关水的说法正确的是( )
| A. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| B. | 将黄河水经沉降、过滤、吸附、杀菌等净化操作后,可供人们生活用水 | |
| C. | 用肥皂水不可以区分硬水和软水 | |
| D. | 水体有一定的自净功能,工业污水可直接排放 |
13.人体不同器官的体液会保持相对稳定的酸碱度范围.由表可知:以下叙述中正确的是( )
| 体 液 | 血 液 | 唾 液 | 胃 液 |
| pH | 7.35~7.45 | 6.6~7.2 | 0.9~1.5 |
| A. | 人的血液一定呈碱性 | |
| B. | 人的胃液一定能使紫色石蕊试液变成蓝色 | |
| C. | 人的唾液一定呈酸性 | |
| D. | 用pH试纸能精确测定以上体液的pH |
16.某同学做了如下图所示实验并对实验数据和现象记录如下表,请回答下列问题: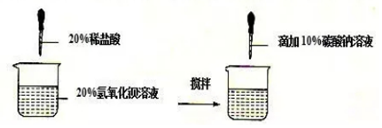
(1)写出第一次实验中加入盐酸后发生反应的化学方程式2HCl+Ba(OH)2═BaCl2+2H2O.
(2)第一次实验结束后所得溶液中溶质的化学式为NaCl和NaOH.
(3)根据已知条件求解出第二次实验生成白色沉淀X的比例式$\frac{106}{21.2g}=\frac{197}{X}$.
(4)第二次实验中每一步所加物质均恰好完全反应
(5)若向第二次的溶液中加入51.4g水,则所得不饱和溶液中溶质的质量分数为5%.
(6)若配制实验中需要的稀盐酸,需用36.5%的浓盐酸的质量为140g.

| 实验次数 | 第一次 | 第二次 | 第三次 |
| 氢氧化钡溶液质量 | 171g | 171g | 171g |
| 滴加盐酸的质量 | 36.5g | 73g | 146g |
| 滴加碳酸钠溶液质量 | 212g | 212g | 212g |
(2)第一次实验结束后所得溶液中溶质的化学式为NaCl和NaOH.
(3)根据已知条件求解出第二次实验生成白色沉淀X的比例式$\frac{106}{21.2g}=\frac{197}{X}$.
(4)第二次实验中每一步所加物质均恰好完全反应
(5)若向第二次的溶液中加入51.4g水,则所得不饱和溶液中溶质的质量分数为5%.
(6)若配制实验中需要的稀盐酸,需用36.5%的浓盐酸的质量为140g.