题目内容
1.实验室制备二氧化碳的实验如下: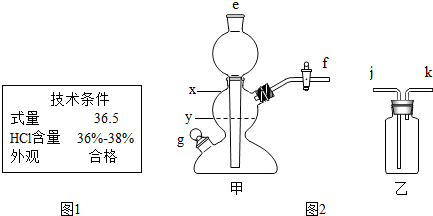
①市售浓盐酸的标签局部见图1,该盐酸中HCl质量分数的范围是36%-38%.为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸稀释.
②用甲装置制备二氧化碳,选择的固体药品是b(选填编号).
a.粉末状石灰石 b.块状大理石 c.粉末状熟石灰 D.块状生石灰
③控制所加盐酸的量,使反应时甲装置内液面位于y处(选填“x”或“y”)为宜.
④收集二氧化碳,应将甲的f处于乙的j处连接(选填有关编号).
⑤写出用澄清石灰水检验二氧化碳的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
⑥反应生成了0.1mol二氧化碳,求稀盐酸中参与反应的HCl的质量.(根据化学方程式列式计算)7.3g.
分析 ①根据标签信息以及控制反应速率的方法来分析;
②根据实验室制取二氧化碳的药品来分析;
③根据药品的量的选择来分析;
④根据二氧化碳的密度来分析;
⑤二氧化碳能和澄清石灰水指导氢氧化钙反应生成碳酸钙沉淀和水;
⑥由生成二氧化碳气体的质量,根据反应的化学方程式计算出HCl的质量.
解答 解:①由试剂瓶标签信息可知,该盐酸中HCl质量分数的范围是36%-38%;为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸进行稀释,反应物的浓度变小,反应速率减慢;故填:36%-38%;稀释;
②在实验室中,通常用大理石或石灰石与稀盐酸反应来制取二氧化碳,粉末状的石灰石与盐酸接触面积过大,反应速率过快;而熟石灰和生石灰与盐酸反应不会生成二氧化碳;故填:b;
③选择的液体药品只要是能将固体药品浸没起来即可;故填:y;
④二氧化碳的密度比空气大,所以收集二氧化碳时,应该从长管进入;故填:f;j;
⑤氢氧化钙和二氧化碳反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;故填:Ca(OH)2+CO2═CaCO3↓+H2O;
⑥0.1mol二氧化碳的质量为:0.1mol×44g/mol=4.4g.
设生成4.4g二氧化碳需要HCl的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
x 4.4g
$\frac{73}{44}=\frac{x}{4.4g}$
x=7.3g
故答案为:7.3g.
点评 本题难度不大,掌握气体的制取与收集方法,根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
11.下列食品中富含蛋白质的是( )
| A. | 鲤鱼 | B. | 黄瓜 | C. | 米饭 | D. | 苹果 |
12.下列实验方案,不合理的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验Cl- | 先加AgNO3溶液,再加稀HNO3 |
| B | 检验CO2 | 用燃着的木条伸入集气瓶内 |
| C | 检验O2 | 用带火星的木条伸入集气瓶内 |
| D | 检验NH4+ | 加NaOH溶液,微热,用湿润的红色石蕊试纸检验生成的气体 |
| A. | A | B. | B | C. | C | D. | D |
9.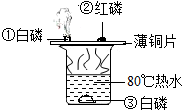 运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
 运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )
运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是( )| A. | ①②现象对比,说明温度达到可燃物的着火点是燃烧条件之一 | |
| B. | ①③现象对比,说明有氧气参与是燃烧条件之一 | |
| C. | 白磷的着火点低于80℃ | |
| D. | 热水只起到加热作用 |
6.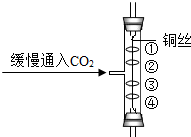 如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球.下列能准确描述实验现象的是( )
如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球.下列能准确描述实验现象的是( )
 如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球.下列能准确描述实验现象的是( )
如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球.下列能准确描述实验现象的是( )| A. | ④比①先红,②、③不变红 | B. | ①比④先红,②、③不变红 | ||
| C. | ④变红,①②③不变红 | D. | ①变红,②③④不变红 |
13.公园里部分植物的枝叶枯黄,茎也比较纤细.建议工作人员最好给这些植物施用的一种化肥是( )
| A. | NH4HCO3 | B. | KNO3 | C. | Ca(H2PO4)2 | D. | (NH4)3PO4 |
10.将O2、C、CO、CuO、Na2CO3、稀硫酸六种物质两两混合,在一定条件下能发生的化学反应有( )
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
13.下列相关事实用微观粒子的知识解释正确的是( )
| 选项 | 亊实 | 解籽 |
| A | 硝酸钾溶液可以导电 | 溶液中存在自由移动的电子 |
| B | 金刚石和石墨燃烧的产物相同 | 碳原子排列方式相同 |
| C | 水银温度计受热示数上升 | 温度升高,汞原子的间隔变大 |
| D | 酒精具有挥发性 | 酒精分子具有挥发性 |
| A. | A | B. | B | C. | C | D. | D |