题目内容
17.过碳酸钠(Na2CO4)是一种常见的漂白杀菌剂,工业用的过碳酸钠往往含有少量的碳酸钠.为了测定过碳酸钠的纯度,某同学在资料中获悉:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O.他们进行了下列研究,请完成有关问题:(1)取2.8g样品与足量的稀盐酸反应,只要测定反应过程中产生的氧气气体体积,就可推算出过碳酸钠的纯度.
(2)请选取需要的装置,并写出这些装置的正确连接顺序BEDCFG(填字母).
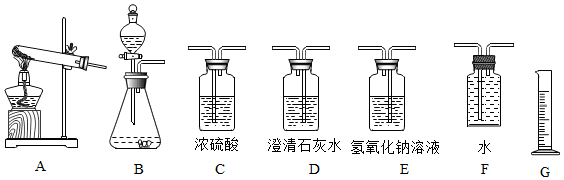
分析 (1)由题给反应方程式可知,过碳酸钠和盐酸反应生成二氧化碳和氧气,碳酸钠和盐酸反应也有二氧化碳生成,所以只能通过测生成氧气的量求过碳酸钠的量;
(2)根据反应物的状态和反应条件选择反应发生装置;根据实验思路,要测生成氧气的量,可用排水法,必须先除去生成的二氧化碳,由此选择实验装置;
解答 解:(1)过碳酸钠和盐酸反应生成二氧化碳和氧气,碳酸钠和盐酸反应也有二氧化碳生成,所以只能通过测生成氧气的量求过碳酸钠的量;
故答案为:氧气;
(2)过碳酸钠和盐酸反应为固体和液体反应且不需要加热,故选择装置B.要测定生成氧气的量,需要先除去二氧化碳,可用氢氧化钠溶液吸收二氧化碳,澄清石灰水检验,浓硫酸干燥,再通入水中,F量筒中水的体积即为E装置中氧气排开水的体积,二者体积相等.
故答案为:BEDCFG.
点评 本题考查化学实验的装置连接及判断反应物过量问题,解题时要注意反应发生装置的选取依据的原则是反应物状态和反应条件、实验设计要注意语言描述的准确性,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
12.有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
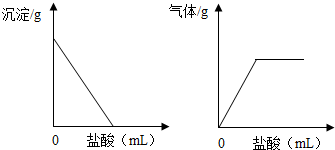

| A. | 肯定只存在Na2CO3 | B. | 可能存在Na2SO4 | ||
| C. | 肯定不存在BaCl2 | D. | 可能存在NaOH |
2.下列物质中,同种元素的化合价都相同的一组是( )
| A. | K2MnO4 KMnO4 | B. | P2O5 Ca3(PO4)2 | C. | NH4Cl HNO3 | D. | Cl2 CaCl2 |
6.原子中决定相对原子质量大小的主要微粒是( )?
| A. | 质子 | B. | 质子数 | C. | 质子和中子 | D. | 质子数和中子数 |
