题目内容
4.有A、B、D三种金属元素.将A、B、D三种单质分别放入稀盐酸中,只有D表面有气泡冒出;将A、B两种金属片分别放入硫酸铜溶液中,B表面析出红色金属,A没有明显现象.据此判断,三种金属的活动性由强到弱的顺序是( )| A. | A>B>D | B. | D>B>A | C. | D>A>B | D. | B>A>D |
分析 根据金属与酸或盐的反应规律,利用甲、乙、丙三种金属及其化合物间可发生的反应,推断甲、乙、丙三种金属活动性由强至弱的顺序.
解答 解:根据题意,将A、B、D三种金属分别放入稀盐酸中,只有D表面产生气泡可判断三种金属中D的活性性最强;把A、B分别放入硫酸铜溶液中,B表面有红色物质析出,A表面无明显现象,说明B的活动性比铜强而A比铜弱,即金属B的活动性比A强;故三种金属的活动性顺序为D>B>A;
故选B.
点评 金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
14.下列有关说法错误的是( )
| A. | 为防止森林大火蔓延可开挖隔离带,其目的是隔绝可燃物 | |
| B. | 肥皂水可以将硬水转化为软水 | |
| C. | 大量焚烧秸秆会加剧对空气的污染 | |
| D. | 氮气用来保护粮食,是利用氮气常温下化学性质稳定 |
15.下列各组物质发生的变化,均属于化学变化的是( )
| A. | 牛奶变质;石油分馏 | |
| B. | 汽油挥发;用盐酸除铁锈 | |
| C. | 生石灰遇水放热;镁带在空气中燃烧后变为白色粉末 | |
| D. | 用木炭除去冰箱中的异味;给水通直流电 |
19.小燕同学通过初中化学的学习,发现物质的名称并不是都能够反映物质的组成与结构.以下的结论不正确的是( )
| A. | 干冰不是冰 | B. | 食盐不是盐 | C. | 铅笔不含铅 | D. | 纯碱不是碱 |
9. 已知,电磁铁的磁性随电流的增大而增强.如图,开关闭合后,电源电压保持不变,弹簧秤下挂着一块磁铁.现在盛有氢氧化钡溶液的烧杯中,逐渐滴入硫酸铜溶液至过量,可发现弹簧秤的示数( )
已知,电磁铁的磁性随电流的增大而增强.如图,开关闭合后,电源电压保持不变,弹簧秤下挂着一块磁铁.现在盛有氢氧化钡溶液的烧杯中,逐渐滴入硫酸铜溶液至过量,可发现弹簧秤的示数( )
 已知,电磁铁的磁性随电流的增大而增强.如图,开关闭合后,电源电压保持不变,弹簧秤下挂着一块磁铁.现在盛有氢氧化钡溶液的烧杯中,逐渐滴入硫酸铜溶液至过量,可发现弹簧秤的示数( )
已知,电磁铁的磁性随电流的增大而增强.如图,开关闭合后,电源电压保持不变,弹簧秤下挂着一块磁铁.现在盛有氢氧化钡溶液的烧杯中,逐渐滴入硫酸铜溶液至过量,可发现弹簧秤的示数( )| A. | 一直保持不变 | B. | 先变大,后变小,最后趋于稳定 | ||
| C. | 先变小,后变大,最后趋于稳定 | D. | 逐渐变大,最后趋于稳定 |
13.下表为各物质所含的少量杂质以及除去这些杂质应选用的试剂或操作方法.正确的一组为( )
| 序号 | 物 质 | 杂 质 | 除杂质应选用的试剂或操作方法 |
| ① | Cu | Fe | 加入足量稀盐酸,充分反应后,过滤、洗涤、干燥 |
| ② | 氮气 | 氧气 | 通过足量的灼热的铜网 |
| ③ | CO2 | HCl、H2O | 依次通过盛有足量饱和NaHCO3溶液和浓硫酸的洗气瓶 |
| ④ | NaCl溶液 | CaCl2、MgCl2、Na2SO4 | 依次加入过量的BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后过滤,再滴加稀盐酸调节溶液pH为7 |
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ①②④ |
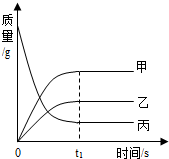 如图反映了某个化学反应各物质质量与时间的关系.
如图反映了某个化学反应各物质质量与时间的关系.