题目内容
11.金属的冶炼与回水使资源得到了充分利用.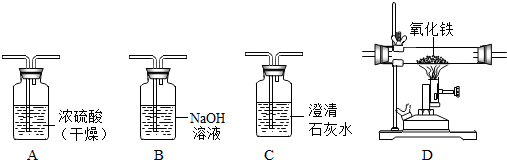
①火法炼铁的原理是Fe2O3+3CO$\stackrel{高温}{→}$2Fe+3CO2,实验室有不纯的CO(混有CO2和水蒸气,若要用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,下述装置的正确连接顺序为(假设每步均完全反应,装置不得重复使用):不纯的CO→B、A、D、C(填字母).
②湿法炼铜的原理是用稀硫酸将矿石中的氧化铜溶解,然后用较活泼的金属置换出铜.将0.2 mol铁粉放入足量硫酸铜溶液中,理论上能生成12.8g铜(根据化学方程式计算).
③现欲从含有CuSO4的废液中回收铜,同时得到工业原料-硫酸亚铁晶体,设计方案如下:
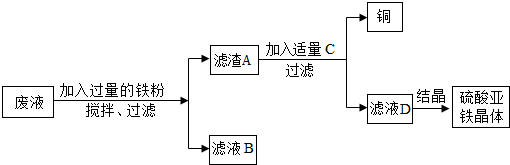
Ⅰ、滤渣A的成分是Fe和Cu,C物质是H2SO4.
Ⅱ、从提高硫酸亚铁晶体回收率的角度分析,该方案的一个不足之处是没有将滤液B中的硫酸亚铁进行回收.
④上述铜的冶炼和回收过程中,铜元素存在形态的变化是B.
A.游离态→化合态 B、化合态→游离态.
分析 ①根据一氧化碳还原氧化铁的原理,反应生成二氧化碳,能使澄清石灰水变浑浊,而一氧化碳中混有二氧化碳和水,除二氧化碳可用碱反应吸收,水可用任意干燥剂,一氧化碳有毒,最终要进行尾气的处理;
②根据化学方程式进行计算;
③在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,故要回收铜得到硫酸亚铁,可以加入铁;
④由硫酸铜转化为单质铜.
解答 解:①除二氧化碳用碱液,除水用浓硫酸,除二氧化碳时所用试剂液体,也会带出水蒸气,故除杂质气体在前、干燥气体在后,检验产物二氧化碳用澄清石灰水,故答案为:B、A、D、C;
②设理论上可产生铜的质量为x
Fe+CuSO4=Cu+FeSO4
1mol 64
0.2mol x
$\frac{1mol}{64}=\frac{0.2mol}{x}$
x=12.8g
故填:12.8
③向废液中加入过量的铁粉,过滤后得到的滤渣A是铜和铁的混合物;分离铁和铜的混合物,可以加入适量的酸--稀硫酸;滤液B中也含有硫酸亚铁,也应该回收.
故答案为:Ⅰ、Fe和Cu;H2SO4
Ⅱ、没有将滤液B中的硫酸亚铁进行回收;
④此过程实现了由硫酸铜这种化合物向铜这种单质的转化,是由化合态变成游离态.故填:B.
点评 本题考查了铜的回收,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列关于CO2和CO的比较错误的是( )
| A. | CO2可用于光合作用,CO可用于人工降雨 | |
| B. | CO2能溶于水,CO难溶于水 | |
| C. | 1个二氧化碳分子比一氧化碳分子多一个氧原子 | |
| D. | CO2会造成温室效应,CO易与血液中血红蛋白结合引起中毒 |
2.t1℃时,分别将20g甲、乙两固体分别放入盛有100g水的两烧杯中,都恰好完全溶解(如图1).当两种溶液升温到t2℃时,两个烧杯中出现如图2所示的现象.根据上述实验,结合图中甲、乙两物质的溶解度曲线,下列说法正确的是( )


| A. | t1℃时烧杯中甲、乙两物质形成的溶液是不饱和溶液 | |
| B. | t2℃时乙物质的溶解度是130g | |
| C. | t2℃时烧杯中甲物质溶液的质量是110g | |
| D. | t1℃时烧杯中甲、乙两物质形成的溶液溶质质量分数约为16.7% |
19.加湿器可增加室内空气湿度,这是因为( )
| A. | 分子体积很小 | B. | 分子间有间隔 | C. | 分子发生分解 | D. | 分子不断运动 |
6.现有一包混有少量氯化钠的硝酸钾固体,通过如下实验提纯硝酸钾,其中错误的是( )
| A. |  溶解 | B. |  蒸发浓缩 | C. |  降温结晶 | D. |  过滤 |
16.卫生部门建议,对高度怀疑或已确诊H7N9型禽流感病例尽早使用“达菲”抗流感药物.达菲的化学式是C16H31N2PO8,则下列说法正确的是( )
| A. | 达菲是由5种元素组成的混合物 | |
| B. | 达菲是有机化合物 | |
| C. | 达菲相对分子质量为410g | |
| D. | 达菲中碳、氢两种元素的质量比是16:31 |
20.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
1.除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
| 编号 | 物质 | 杂质 | 试剂 | 除杂操作方法 |
| A | CO | CO2 | 氧化铜 | 加热 |
| B | CaO | CaCO3 | 水 | 过滤、蒸发 |
| C | MnO2 | KCl | 水 | 溶解、过滤、洗涤、烘干 |
| D | NaCl | KNO3 | 水 | 溶解、蒸发浓缩、冷却结晶、过滤、洗涤、烘干 |
| A. | A | B. | B | C. | C | D. | D |
 (1)配制10%的盐酸的步骤有:
(1)配制10%的盐酸的步骤有: