题目内容
14.活泼金属能与某些非金属单质、酸溶液,某些盐溶液反应,其中金属与酸溶液、某些盐溶液属于置换反应;非金属单质(如ⅧA中的Cl2、Br2和I2)与某些盐溶液反应也有类似的规律.(1)根据下列反应:Cl2+2NaBr═2NaCl+Br2;Br2+2KI═2KBr+I2.答下列问题:
①Cl2、Br2和I2的活泼性由弱到强的顺序是I2<Br2<Cl2;
②下列化学反应能发生的是A(填序号)
A.2NaCl+I2═2NaI+Cl2 B.2KI+Cl2═2KCl+I2 C.Br2+2NaCl=2NaBr+Cl2
③査阅资料得知硫的活泼性比上述三种单质都弱,请用一个化学方程式证明此结论:I2+Na2S=S+2NaI;
(2)已知F与Cl、Br和I为同一族元素,但F2与其它几种元素的盐溶液不能发生置换反应,却能与水在常温下发生置换反应,写出该反应的化学方程式2F2+2H2O=4HF+O2.
分析 (1)①根据非金属单质与某些盐溶液反应比较非金属活泼性强弱.
②根据非金属活泼性强弱分析判断;
③根据题意可得,非金属单质和盐反应具有和金属类似的规律,即活动性强的非金属可以把活动性弱的非金属置换出来.
(2)根据题干反应分析反应物、生成物,写出反应的化学方程式.
解答 解:(1)①由Cl2+2NaBr═2NaCl+Br2可知,非金属的活动性是:Br2<Cl2;由Br2+2KI═2KBr+I2可知,非金属的活动性是:I2<Br2.由此可知,Cl2、Br2和I2的活泼性由弱到强的顺序是I2<Br2<Cl2;
②A.由于I2<Cl2,2NaCl+I2═2NaI+Cl2能发生;
B.由于I2<Cl2,2NaCl+I2═2NaI+Cl2不能发生;
C.由于Br2<Cl2,Br2+2NaCl=2NaBr+Cl2不能发生.
③由于S的活动性比I2、Br2、Cl2都弱,所以应该选用最弱的一个进行实验.即选用碘单质和硫化钠等反应,方程式是:I2+Na2S=S+2NaI.
(2)由题意可知,F2能与水在常温下发生置换反应,生成了氟化氢和氧气,该反应的化学方程式是:2F2+2H2O=4HF+O2.
故答为:(1)①I2<Br2<Cl2;②A..③I2+Na2S=S+2NaI;(2)2F2+2H2O=4HF+O2.
点评 本题考查的是金属的性质以及非金属性的判断,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
4.某学生用托盘天平称量食盐,错将砝码与食盐位置放倒,现在砝码为5克,游码为0.5克,则托盘中食盐为( )
| A. | 5克 | B. | 5.5克 | C. | 4.5克 | D. | 4克 |
5.膨松剂是一种食品添加剂,某研究小组对膨松剂进行了如下探究
【趣味实验】
实验1:和面.向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10mL水,再加入2g膨松剂M,制得的面团编为2号.
实验2:发面.将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软.
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是NH4HCO3;
假设2:M是NaHCO3;
假设3:M是NH4HCO3和NaHCO3
【实验探究1】
【提出新问题】实验①试管中剩余固体是什么?
【实验探究2】
实验②:将实验①所得固体继续加热,无明显现象.冷却,向试管中加水,固体全部溶解,将所得溶液分为2份;向其中1份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀;向另1份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红.
【得出结论】
实验①试管中剩余固体是Na2CO3(填化学式)
【反思提高】
(1)NH4HCO3受热分解的化学方程式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(2)受热稳定性:Na2CO3>(填“>”“=”或“<”)NaHCO3.
【拓展应用】
某品牌复配膨松剂N的配料为:磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应:Ca(H2PO4)2+2NaHCO3═CaHPO4↓+Na2HPO4+2CO2↑+2H2O;利用N和面和发面(加热)时,面团都会胀大.下列叙述正确的是abc(填序号)
a.常温下的溶解度:Na2HPO4>CaHPO4
b.碳酸氢钠在水溶液中遇到酸性物质能产生气体
c.根据上述反应,产生0.22gCO2至少需要NaHCO3的质量为0.42g.
【趣味实验】
实验1:和面.向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10mL水,再加入2g膨松剂M,制得的面团编为2号.
实验2:发面.将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软.
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是NH4HCO3;
假设2:M是NaHCO3;
假设3:M是NH4HCO3和NaHCO3
【实验探究1】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取少量M于试管中,加热一段时间 | 无刺激性气味 试管内壁有水珠 试管内有固体剩余 | 假设2成立 假设1、3不成立 |
【实验探究2】
实验②:将实验①所得固体继续加热,无明显现象.冷却,向试管中加水,固体全部溶解,将所得溶液分为2份;向其中1份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀;向另1份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红.
【得出结论】
实验①试管中剩余固体是Na2CO3(填化学式)
【反思提高】
(1)NH4HCO3受热分解的化学方程式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
(2)受热稳定性:Na2CO3>(填“>”“=”或“<”)NaHCO3.
【拓展应用】
某品牌复配膨松剂N的配料为:磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应:Ca(H2PO4)2+2NaHCO3═CaHPO4↓+Na2HPO4+2CO2↑+2H2O;利用N和面和发面(加热)时,面团都会胀大.下列叙述正确的是abc(填序号)
a.常温下的溶解度:Na2HPO4>CaHPO4
b.碳酸氢钠在水溶液中遇到酸性物质能产生气体
c.根据上述反应,产生0.22gCO2至少需要NaHCO3的质量为0.42g.
19.下列物质的名称、俗称、化学式不完全对应的是( )
| A. | 汞 水银 Hg | B. | 固态二氧化碳 干冰 CO2 | ||
| C. | 氢氧化钠 烧碱 NaOH | D. | 碳酸氢钠 苏打 NaHCO3 |
6.生活中的下列变化过程发生了化学变化的是( )
| A. | 二氧化碳常用作气体肥料 | B. | 用秸秆、粪便等发酵制得沼气 | ||
| C. | 净水滤芯内填充活性炭净水 | D. | 排放到空气中的二氧化硫形成酸雨 |
4.下列说法正确的是( )
| A. | 金刚石与石墨的化学性质相同,是因为分子结构相同 | |
| B. | 水和过氧化氢的化学性质不同,是因为原子的结构不同 | |
| C. | 稀硫酸与盐酸的化学性质完全相同,是因为酸中都有氢离子 | |
| D. | 钠原子与钠离子的化学性质不同,是因为最外层的电子数不同 |
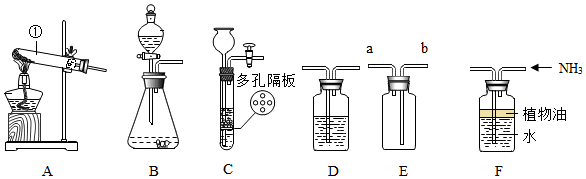
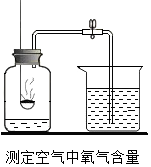 如图是测定空气中氧气含量的实验装置,请据图回答下列问题:
如图是测定空气中氧气含量的实验装置,请据图回答下列问题: