题目内容
2.有一种可能含下列物质的硝酸铵样品中,经分析知道其中氮元素的质量分数为20%,那么该样品中(括号内数字为相应物质氮元素质量分数)一定含有下列物质是( )| A. | NH4HCO3 | B. | CO(NH2)2 | C. | (NH4)2 SO4 | D. | NH4 Cl |
分析 可以求出硝酸铵中氮元素的质量分数,如果硝酸铵中氮元素的质量分数大于20%,则含有的氮肥中氮元素的质量分数应该小于20%.
解答 解:硝酸铵中氮元素的质量分数为:$\frac{28}{80}$×100%=35%.
通过计算可知,碳酸氢铵中氮元素的质量分数是17.7%,尿素中氮元素的质量分数是46.7%,硫酸铵中氮元素的质量分数是21.2%,氯化铵中氮元素的质量分数是26.2%.
当含有的杂质的氮肥含氮量为20%时,由于硝酸铵的含氮量为35%,所以对应的杂质的含氮量必须低于20%,所以只能为碳酸氢铵.
故选A.
点评 解答本题要掌握物质中每种元素的质量分数的求法,通过计算得出的数据进行分析、判断,从而得出正确的结论.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
13.空气中氮气和氧气的体积比约为( )
| A. | 1:5 | B. | 5:1 | C. | 1:4 | D. | 4:1 |
10.氢气和氧气的混合气体5g,点燃使之充分反应,得到2.7g水,则反应前混合气体中氧气的质量可能是( )
| A. | 0.3g | B. | 2.4g | C. | 2.6g | D. | 4.7g |
7.市场上销售的加碘食盐、含氟牙膏、高钙牛奶、补铁酱油等,这里的碘、氟、钙、铁是指( )
| A. | 单质 | B. | 分子 | C. | 元素 | D. | 原子 |
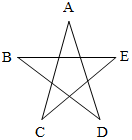 A、B、C、D、E五种物质均为初中化学中常见的化合物,它们之间的关系如图所示,相互之间连线表示两者间能发生化学反应.A、C、E均为氧化物,A是人体呼出的主要气体,常用于灭火;B是人体中胃液的主要成分,可用于除铁锈,而D溶液可以用来检验A;C和E反应能生成D.
A、B、C、D、E五种物质均为初中化学中常见的化合物,它们之间的关系如图所示,相互之间连线表示两者间能发生化学反应.A、C、E均为氧化物,A是人体呼出的主要气体,常用于灭火;B是人体中胃液的主要成分,可用于除铁锈,而D溶液可以用来检验A;C和E反应能生成D.
