题目内容
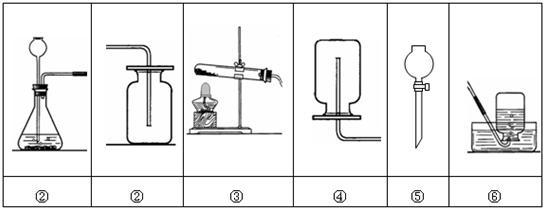
化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据下图回答有关问题:(第

(1)从上述仪器中选择一种你比较熟悉的仪器,写出它的名称________,简要写出它的用途________.
(2)在常温上实验室欲制氧气所选用的装置是________(填序号),为了便于调控反应的进行,可以对发生装置进行改进,请简要说明你的改进措施________.
(3)请写出一种用③装置制取氧气的符号表达式:________;用排水法收集一瓶氧气,发现不纯,可能的原因是________(答出一点即可).
(4)实验室制取下列气体,可以用①装置作为发生装置的是________(填序号)
A.电石(固体)和水在常温下反应制乙炔气体
B.浓盐酸和二氧化锰共热制氯气C.石灰石与稀盐酸常温下制二氧化碳
(5)与高锰酸钾(或氯酸钾和二氧化锰的混合物)制取氧气相比,用过氧化氢制取氧气的优点是________.
解:(1)长颈漏斗,方便加液体药品,本题开放性比较强,合理即可,故答案为:长颈漏斗;方便加液体药品
(2)在常温上实验室欲制氧气所选用的装置是:①②或①⑥;分液漏斗与长颈漏斗相比的优点是:便于调控反应的进行.故答案为:①②或①⑥;把长颈漏斗改为分液漏斗
(3)用③装置制氧气时需要用高锰酸钾或氯酸钾,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气.用排水法收集一瓶氧气,发现不纯,可能是收集氧气过早.故答案为:KMnO4 K2MnO4+MnO2+O2;收集氧气过早
K2MnO4+MnO2+O2;收集氧气过早
(4)用①装置的条件是:固体和液体在常温下反应,故答案为:A、C;
(5)用过氧化氢制取氧气的优点是:不需加热,节约能源.故答案为:不需加热,节约能源
分析:如果用过氧化氢和二氧化锰制氧气,就不需要加热;如果用高锰酸钾或氯酸钾就需要加热.氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集.分液漏斗比长颈漏斗便于调控反应的进行;用过氧化氢制取氧气的优点是:不需加热,节约能源.
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了符号表达式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.
(2)在常温上实验室欲制氧气所选用的装置是:①②或①⑥;分液漏斗与长颈漏斗相比的优点是:便于调控反应的进行.故答案为:①②或①⑥;把长颈漏斗改为分液漏斗
(3)用③装置制氧气时需要用高锰酸钾或氯酸钾,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气.用排水法收集一瓶氧气,发现不纯,可能是收集氧气过早.故答案为:KMnO4
 K2MnO4+MnO2+O2;收集氧气过早
K2MnO4+MnO2+O2;收集氧气过早(4)用①装置的条件是:固体和液体在常温下反应,故答案为:A、C;
(5)用过氧化氢制取氧气的优点是:不需加热,节约能源.故答案为:不需加热,节约能源
分析:如果用过氧化氢和二氧化锰制氧气,就不需要加热;如果用高锰酸钾或氯酸钾就需要加热.氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集.分液漏斗比长颈漏斗便于调控反应的进行;用过氧化氢制取氧气的优点是:不需加热,节约能源.
点评:本考点主要考查气体的制取装置和收集装置的选择,同时也考查了符号表达式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
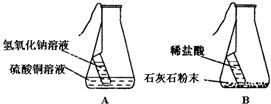


 化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题:
化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题:




