题目内容
现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:(1)当反应进行到A点时,生成二氧化碳的质量.
(2)石灰石样品中碳酸钙的质量分数.

【答案】分析:(1)根据图象可以看出,A点表示的含义是加入146克盐酸生成的二氧化碳的质量.
(2)写出化学方程式并代入盐酸(溶质)的质量计算出碳酸钙的质量.
解答:解:(1)盐酸(溶质)的质量=146克×10%═14.6克,设生成二氧化碳的质量为X,石灰石样品中碳酸钙的质量为Y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
Y 14.6克 X
 ═
═
得:Y=20克
 ═
═
得:X=8.8克
(2)由(1)计算可知,碳酸钙的质量是20克,所以石灰石样品中碳酸钙的质量分数= ×100%=80%.
×100%=80%.
答:生成二氧化碳的质量为8.8g,石灰石样品中碳酸钙的质量分数为80%.
点评:掌握化学方程式的计算格式和规范性,学会看图象并从中得到一些信息的方法.
(2)写出化学方程式并代入盐酸(溶质)的质量计算出碳酸钙的质量.
解答:解:(1)盐酸(溶质)的质量=146克×10%═14.6克,设生成二氧化碳的质量为X,石灰石样品中碳酸钙的质量为Y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
Y 14.6克 X
 ═
═
得:Y=20克
 ═
═
得:X=8.8克
(2)由(1)计算可知,碳酸钙的质量是20克,所以石灰石样品中碳酸钙的质量分数=
 ×100%=80%.
×100%=80%.答:生成二氧化碳的质量为8.8g,石灰石样品中碳酸钙的质量分数为80%.
点评:掌握化学方程式的计算格式和规范性,学会看图象并从中得到一些信息的方法.

练习册系列答案
相关题目
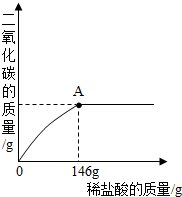 现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:
现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求: 现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求:
现取25g石灰石样品,加入溶质质量分数为10%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应).求: